Содержание в природе
Как самостоятельный элемент цинк в природе не встречается. Его можно добыть из 66 минералов, среди которых сфалерит, каламин, франклинит, цинкит, виллемит, смитсонит. Первый является наиболее распространенным источником металла, его часто называют «цинковой обманкой». Он состоит из сульфида цинка и примесей, которые придают минералу разнообразные цвета. Это осложняет его поиск и правильное определение.
Найти цинк можно в кислых и изверженных породах — во последних его немного больше. Часто металл в виде сульфида вместе со свинцом встречается в термальных водах, мигрирует в поверхностных и подземных источниках.
В живых организмах
В теле человека содержится около 2 граммов цинка, около 400 ферментов содержат его. К последним относятся ферменты, катализирующие гидролиз белков, сложных эфиров и лептидов, полимеризацию РНК и ДНК, образование альдегидов. Чистый элемент содержится в мышцах, поджелудочной железе и печени. В день мужчинам требуется 11 мг цинка, женщинам — 8 мг.
В организме цинк выполняет следующие функции:
- Нормализует деятельность простаты;
- Способствует метаболизму витамина Е;
- Принимает участие в синтезе анаболических гормонов: гормоне роста, инсулине, тестостероне и других;
- Участвует в продукции мужских гормонов и спермы;
- Помогает расщепить алкоголь в организме.
При недостатке элемента в организме наблюдается быстрая утомляемость, раздражительность, потеря памяти, снижение зрения и веса без объективной причины, приступы аллергии, депрессивное состояние. Происходит понижение уровня инсулина и накопление в теле некоторых элементов: железа, свинца, меди, кадмия.
4.3.2 Свинец
Основным потребителем свинца и его сплавов в России является
промышленность по выпуску аккумуляторов.
Почти 90% запасов металла РФ сконцентрировано в Сибири, еще 7% — на
Дальнем Востоке. Около 70% российских запасов свинца сосредоточено в двух
регионах на трех крупнейших месторождениях: Горевском в Красноярском крае
(почти 44% разведанных запасов), Озерном и Холоднинском в Республике
Бурятия.
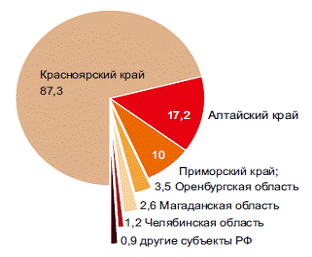
Рис. 4.3.3. Распределение добычи свинца по субъектам РФ в 2009 г., тыс. т
Доля страны в мировой добыче свинца в 1995 г. составляла 0,9%, в 2000 г.
— 0,4%, а в 2008 г. — достигла почти 1,4%. Доля России в мировом производстве
рафинированного свинца в 1995 г. равнялась 0,55%, в 2000 г. — 0,7%, а в 2008 г.
— поднялась до 1,15%. Таким образом, за счет наращивания выпуска вторичного
металла роль страны в мировом выпуске рафинированного свинца растет, при этом
добываемая свинцовая руда не является востребованной плавильными предприятиями
Кавказа, Урала, Восточной Сибири и Приморского края.
В экспортных отгрузках рафинированных свинца и цинка для России главным
являются турецкий рынок, на который в 2009 г. приходилось 25% суммарного вывоза
металла, и рынок Германии (20,6%). В крупных масштабах осуществлялись также
поставки в страны СНГ (в 2009 г. — около 11%, в 2008 — 23%): в основном на
Украину (8 тыс. т), Узбекистан (0,77 тыс.) и Казахстан (0,1 тыс.). В 2004 —
2008 гг. постепенно росла доля КНР — с 2,2 до 6,2%, однако в 2009 г. она
уменьшилась до 5,6%.
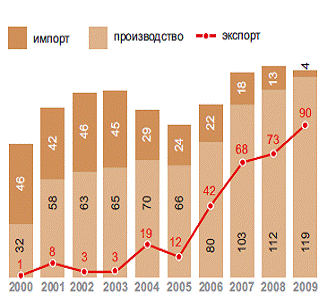
Рис. 4.3.4. Динамика производства, экспорта и импорта рафинированного
свинца в 2000-2009 гг., тыс. т
Рафинированный свинец из РФ уже в течение многих лет поступает на внешние
рынки по ценам ниже среднемировых, но отмечается тенденция к постепенному
приближению к ним.
Заключение
Свинец и цинк — металлы, на долю главных минералов
которых приходится свыше 90 и 95 % запасов и добычи соответственно. В природе
известно более 300 минералов, содержащих свинец, и более 140 — цинк.
Главнейшими минералами свинца и цинка являются сульфиды, сульфосоли и
карбонаты.
Выделяют несколько генетических типов
свинцово-цинковых месторождений: докембрийские колчеданно-полиметаллические,
фанерозойские колчеданно-полиметаллические, свинцово-цинковые (стратиформные),
скарновые и метасоматические залежи в известняках, жильные.
Промышленное использование свинцово-цинковых руд возможно только после
обогащения, преимущественно флотации.
Требования к свинцовым и цинковым концентратам в
каждом конкретном случае регламентируется договором между поставщиком и
перерабатывающими металлургическими и химическими заводами или существующими
ГОСТами и техническим условиями.
Свинцово-цинковая промышленность имеет весомое значение для отечественной
экономики, что непосредственно ведет к увеличению спроса на это сырье.
Список
литературы
1. Государственный доклад «О состоянии и использовании
минерально-сырьевых ресурсов Российской Федерации в 2009 году». Под редакцией
С.Е. Донского. Составление и оформление: Центр «Минерал» ФГУ НПП
«Аэрогеология», 2010 г.
2. Методические рекомедации по применению классификации
запасов к месторождениям свинцовых и цинковых руд. «Государственная комиссия по
запасам полезных ископаемых» (ФГУ «ГКЗ») Москва, 2005 г.
. Рудные месторождения СССР В 3-х т. Под редакцией
академика В. И. Смирнова. Изд. 2-е, перераб. и доп. Т. 2. М., «Недра», 1978.
3928 с.
. «Лондонская биржа металлов» http://www.lme.com
. Ресурсы Интернет
Свойства сплавов цинка
Чтобы понимать какими свойствами должны обладать цинковые сплавы, необходимо знать характеристики цинка. Литейные качества, температура плавления, твердость и другие параметры этого соединения зависят от химических и физических свойств цинка. Он представляет собой голубоватый металл. Это вещество не встречается в природных месторождениях в чистом виде. В процессе длительной обработки получается оксид цинка, из которого можно получить чистый металл.
Характеристики и свойства цинка
Перед описанием сплавов цинка и их применения в различных направлениях производства требуется разобраться со свойствами цинка.
Химические свойства:
- При длительном нагревании может вступать в реакции с Н2О и сероводородом. В ее процессе выделяется водород.
- Не вступает в контакт с углеродом и азотом.
- Смешивается с различными неметаллами — кислородом, фосфором и серой.
- При соединении с щелочами, образуются цинкаты (это соли цинковой кислоты).
- Если смешивать металл с серной кислотой, могут образовываться различные вещества. Все зависит от количества кислоты.
- При очень высокой температуре металл может контактировать с различными газами (йод в газообразном состоянии, хлор и фтор).
Физические свойства:
- Представляет собой прочный металл. При нагревании до 100–150°С он становится пластичным. При разогревании более 210 °С металл изменяет свою форму. В сравнении с другими металлами цинк плавится при низкой температуре.
- Обладает хорошей теплопроводностью — 116 Вт/м К.
- Кипение материала при температуре — 906°С.
- Плотность — 7.133 гр./см куб.
- Плавление материала — 419°С.
- Максимальная прочность при растяжении — 200–250 МН/м2.
- Удельная теплота испарения — 114.8 КДж/моль.
Количество примесей в составе металла напрямую зависит от способа добычи, обработки и изначальной породы материала. Часто встречающиеся примеси, содержащиеся в цинке — никель, фтор, хлор и свинец.

Необработанный металл
Как примеси изменяют свойства цинка
Посторонние примеси, содержащиеся в цинке, ухудшают характеристики этого металла (при большом содержании). Первостепенная задача производителей — снизить количество свинца, кадмия и олова в этом металле, чтобы избежать межкристаллической коррозии.
Воздействие примесей на цинк:
- Свинец — усиливает растворимость металла в воде.
- Медь — ухудшает показатель пластичности. Металл становится более уязвимым для коррозии, однако улучшается его прочность.
- Мышьяк — ухудшает прочность и пластичность цинка даже при минимальном содержании.
- Олово — увеличивает ломкость готовых отливок.
- Кадмий — снижает пластичность металла.
- Сурьма — в процессе прокатки при больших температурах, увеличивает прочность и ухудшает пластичность цинка.
Практически все примеси считаются вредными для готовых заготовок. Из-за этого производители в первую очередь проводят ряд процедур, чтобы содержание цинка в готовой отливке было наиболее высоким.
Цинк
Цинк (Zn) — серебристый металл белого цвета (tпл=420 °С, tкип=906 °С), хрупкий при комнатной температуре. При хранении на воздухе он приобретает лёгкий голубоватый оттенок, покрываясь тонкой плёнкой оксида цинка ZnO или основного карбоната 2ZnCO3•Zn(OH)2, предохраняющей его от дальнейшего окисления.
Цинком покрывают кровельное железо
Обратите внимание на проржавевшую решётку, которая не была оцинкована. Даже если цинковое покрытие будет повреждено, железо всё равно не начнёт ржаветь до тех пор, пока не прокорродирует всё цинковое покрытие
Основная масса цинка идёт на покрытие железа для защиты его от ржавчины. Из оцинкованного железа изготовляют кровельные листы, водосточные трубы, вёдра и многие другие изделия.
Оксид цинка ZnO (tпл=1975 °С) используется как наполнитель для придания прозрачной пластмассе белого цвета, а в смеси с олифой — в качестве белой краски (цинковые белила). Белый порошок сульфида цинка ZnS, в котором часть атомов Zn замещена на Cd, a S на Se, под действием потока электронов излучает видимый свет — тонкий слой этого вещества наносят на экраны телевизоров, рентгеновские трубки.
В организме взрослого человека содержится около 2,3 г цинка, который входит в состав более 40 ферментов, регулирующих углеводный и энергетический обмен в клетках.
Цинк активнее железа, поэтому при контакте отдаёт ему некоторое количество электронов, и поверхность железа заряжается отрицательно. Электроны, которые переходят на кислород с поверхности железа, первоначально принадлежали цинку. Так цинк, разрушаясь сам, защищает железо. Сравнить другие металлы по способности восстанавливать и восстанавливаться можно ознакомившись с .
Химическая реакция, основанная на способности цинка вытеснять ртуть из её соединений, основано действие ртутно-цинкового гальванического элемента. В нём протекает следующий процесс: Zn+HgO=Hg+ZnO.
Ртутно-цинковые элементы не имеют равных по надёжности, стабильности напряжения и количеству «запасённого» электричества в единице массы. Они идеальны для использования в полевых условиях.
Однако ртуть составляет больше половины их массы. После того как батарейки выработают свой ресурс, возникает проблема их утилизации. Если просто выбрасывать такие элементы на свалку, воздух в её окрестностях будет отравлен. Поэтому в мире ширится кампания против использования ртутно-цинковых элементов. В частности, в открытую продажу они уже давно не поступают. А на батарейках, которые продаются в магазинах, можно прочесть: «Mercury 0%» или «Mercury free», что означает «ртути нет».
Латуни — медно-цинковые сплавы (содержат от 4 до 50% Zn) — гораздо прочнее и дешевле меди, более устойчивы к окислению.
Сплавы на основе цинка обладают хорошими литейными качествами. Из них, например, легко отлить гайку с уже готовой резьбой. (Для стали такая возможность пока остаётся несбыточной мечтой.) Поэтому такие сплавы активно используют для отливки изделий с очень тонким рельефом поверхности, например типографских шрифтов.
2.4 Скарновые свинцово-цинковые месторождения
Локализованы преимущественно в карбонатных породах и
приурочены к зонам глубинных разломов, обнаруживая пространственную и временную
связь с малыми интрузиями основного и кислого ряда. Для морфологии рудных тел
типичны значительное разнообразие и сложность: рудные тела трубообразной и иной
сложной формы, приуроченные к участкам пересечения дизъюнктивных нарушений в
карбонатных породах, имеют мощность от нескольких до первых десятков метров,
протяженность — от десятков до нескольких сотен метров; пластообразные и
субпластовые залежи — на контакте карбонатных пород с глинисто-кремнистыми или
алюмосиликатными — имеют размеры до первых сотен метров по простиранию при
мощности в несколько метров; трещинно-жильные тела обычны среди интрузивных и
эффузивных пород. Часто встречаются рудные тела комбинированной формы,
сочетающие в себе элементы всех морфологических типов.
Руды тесно ассоциируют с пироксеновыми и другими
скарнами, участками их окварцевания и хлоритизации, иногда кварц-анкеритовыми
метасоматитами.
Примером месторождений этого типа является
месторождение Алтын-Топкан (рис.2.8).
Месторождение Алтын-Топкан находится в Узбекистане, на
северном склоне гряды Карамазар. Оно приурочено к тектоническому блоку, со всех
сторон ограниченному крупными разломами. Блок сложен карбонатными отложениями
среднего палеозоя, перекрытыми эффузивами верхнего палеозоях отмечается
горизонтальная рудная зональность.
В состав карбонатных пород основания входят слоистые
известняки, доломиты и мергели среднего и верхнего девона, а также массивные
известняки нижнего карбона общей мощностью около 1500 м. Несогласно
перекрывающие их вулканогенные породы верхнего палеозоя состоят из туфов и
туфолав андезитовых порфиритов и липаритовых порфиров мощностью около 800 м.
Породы карбонатной и вулканогенной толщи падают к северо-западу: на юге, близ
контакта с гранодиоритами, под углами 55-60°, а в удалении от него к северу,
под углами 10-15°.
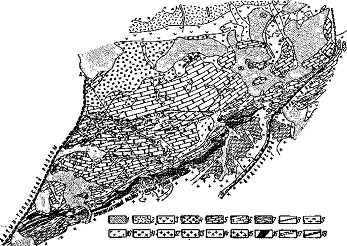
Рис. 2.8. Схематическая геологическая карта
месторождения Алтын-Топкан. По И, Кошла
— четвертичные отложения; 2 — лавы андезитовых
порфиритов; 3 — туфы и туфолавы липаритовых порфиров; 4 — туфы, туфобрекчии и
туфопесчаники андезитовых порфиров; 5 — массивные и грубослоистые известняки; б
— известняки и доломиты; 7 — метаморфизованные терригенные отложения нижнего
палеозоя; 8 — диабазовые порфирита; 9 — кварцевые порфирита; 10 —
гранит-порфиры; 11 — пироксенсодержащие гранодиорит-порфиры; 12 —
крупнопорфировые грано-диорит-порфиры; 13 — сиенитовидные гранодиорит-порфиры;
14 — андезитовидные гранодиорит-порфиры; 15 — гранодиориты; 16 — скарноворудные
тела; 17 — тектонические нарушения; 18 — крупные разломы смятыми в складки,
разбитыми разломами и пронизанными интрузивами верхнего палеозоя.
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
|
DE154695C * |
||||
|
DE208403C * |
||||
|
US2598745A * |
1950-08-25 | 1952-06-03 | New Jersey Zinc Co | Smelting of zinciferous ore |
|
US3094411A * |
1959-04-08 | 1963-06-18 | Bernard H Triffleman | Method and apparatus for the extraction of zinc from its ores and oxides |
|
US3463630A * |
1966-03-03 | 1969-08-26 | Lamar S Todd | Process for producing zinc and related materials |
|
US3892559A * |
1969-09-18 | 1975-07-01 | Bechtel Int Corp | Submerged smelting |
|
FR2430980B1 * |
1978-07-13 | 1980-11-28 | Penarroya Miniere Metall | |
|
GB2048309B * |
1979-03-09 | 1983-01-12 | Univ Birmingham | Method of recovering non-ferrous metals from their sulphide ores |
|
DE3067998D1 * |
1979-03-09 | 1984-07-05 | Nat Res Dev | A method of recovering non-ferrous metals from their sulphide ores |
Применение
В нынешнее время применение сплавов цинка с другими металлами можно увидеть в различных отраслях производства.
Для защиты металлов от коррозии
Чтобы защитить другие металлы от развития коррозии, используется чистый материал, которым покрывается уязвимая поверхность. Процесс покрытия называется металлизация.
В автомобильной отрасли
Цинк и сплавы с его добавлением получили большую популярность в автомобильной отрасли. Смеси металлов используют для декоративного покрытия отдельных элементов автомобиля (ручки, бампера, решетки, зеркала). Зубчатые механизмы, рычажные механизмы, покрышки, аккумуляторах — содержат это вещество.
В производстве ювелирных украшений
Бижутерия и украшения из цинковых сплавов известны уже длительное время. Цинк часто смешивается с золотом. Для изготовления белого золота также используют этот металл. Он осветляет готовое изделие.
В строительстве
В строительстве широкое применение получили сплавы из цинка и других металлов. Например, их используют при производстве кровли. Из оцинковки изготавливается не только кровельное покрытие, но и различные трубы, желоба, ветровые планки, подшивка для свесов крыши.
В медицине
Если говорить о медицине, окись цинка часто используется в качестве антисептического средства. Также ее добавляют в составы использующиеся для ускорения регенерации.

Применение цинка в медицине
В продуктах питания
Элемент имеется в мясе, сыре, кунжуте, устрицах, шоколаде, бобовых, овсянке, подсолнечных и тыквенных семечках, часто присутствует в минеральной воде. Наибольший процент цинка содержится в следующих продуктах (из расчета на 100 грамм):
- Устрицы (до 40 мг), анчоусы (1,72 мг), осьминог (1,68 мг), карп (1,48 мг), икра (до 1 мг), сельдь (около 1 мг).
- Тыквенные семечки (10 мг), кунжут (7 мг), подсолнечные семечки (5,3 мг), арахис (4 мг), грецкие орехи (3 мг), миндаль (3 мг).
- Говядина (до 8,4 мг), баранина (до 6 мг), говяжья печень (4 мг), свинина (до 3,5 мг), курица (до 3,5 мг).
- Какао-порошок без сахара и подсластителей (6,81 мг), чистый горький шоколад (2,3 мг), шоколадные конфеты (до 2 мг в зависимости от количества и вида шоколада).
- Чечевица (4,78 мг), овес (3,97 мг), пшеница (3,46 мг), соевые бобы (3 мг), рожь (2,65 мг), хлеб (до 1,5 мг), зеленый горошек (1,24 мг), горох (1,2 мг), ростки бамбука (1,1 мг), рис (1 мг), злаковое печенье (до 1 мг).
- Твердый сыр (до 4 мг).
Смеси и сплавы
 Для усиления прочности и увеличения температуры плавления металл смешивают с медью, алюминием, оловом, магнием и свинцом.
Для усиления прочности и увеличения температуры плавления металл смешивают с медью, алюминием, оловом, магнием и свинцом.
Самым известным и востребованным сплавом является латунь. Это смесь меди с добавлением цинка, иногда встречаются и олово, никель, марганец, железо, свинец. Плотность латуни достигает 8700 кг/м 3 . Температура, нужная для плавления, держится на отметке 880 C о — 950 C о : чем больше в ней содержание цинка, тем она ниже. Сплав отлично сопротивляется неблагоприятной внешней среде, хоть и чернеет на воздухе, если не покрыта лаком, прекрасно полируется и сваривается контактной сваркой.
Существует два вида латуни:
- Альфа-латунь: более пластична, хорошо гнется в любом состоянии, но сильнее изнашивается.
- Альфа+бета-латунь: деформируется только при нагревании, при этом более износостойка. Часто сплавляют с магнием, алюминием, свинцом и железом. Это позволяет увеличить прочность, но уменьшает пластичность.
Сплав Zamak или Zamac состоит из цинка, алюминия, меди и магния. Само название образовано из первых букв латинских названий: Zink — Aluminium — Magnesium — Kupfer / Cuprum (Цинк-Алюминий-Магний-Медь). В СССР сплав был известен как ЦАМ: Цинк-Алюминий-Медь. Активно применяется в литье под давлением, плавление начинается при низкой температуре (381 C о — 387 C о ) и имеет низкий коэффициент трения (0,07). Обладает повышенной прочностью, что позволяет получать изделия сложной формы, которые не боятся сломаться: дверные ручки, клюшки для гольфа, затворы огнестрельного оружия, строительную фурнитуру, застежки разных видов и рыболовные снасти.
Небольшой процент цинка (не более 0,01%) содержится в гартовых сплавах, применяемых в полиграфии для отливки типографских шрифтов и линеек, печатных форм и машинного набора. Это устаревшие смеси, на место которых пришел чистый цинк с небольшим добавлением примесей.
Невысокая температура, которая требуется для плавления цинка, часто компенсируется за счет сплавов с другими металлами, но бывает и наоборот. Если температура, необходимая для плавления «чистого» металла, составляет 419,5 C о , то сплав с оловом снижается до 199 C о , а с оловом и свинцом — до 150 C о . И хотя такие сплавы можно паять и варить, чаще всего смеси с цинком применяют только для заделки имеющихся дефектов из-за их слабой прочности. Например, сплав олова, свинца и цинка рекомендуется применять только на никелированных изделиях.
Чаще всего цинковые сплавы применяют для создания карбюраторов, рам спидометров, радиаторных решеток, гидравлических тормозов, насосов и декоративных элементов, деталей для стиральных машин, миксеров и кухонного оборудования, часовых корпусов, пишущих машинок, кассовых аппаратов и бытовой техники. Эти детали нельзя применять в промышленном производстве: при повышении температуры до 100 C о прочность изделия снижается на треть, а твердость — почти на 40%. При понижении температуры до 0 C о цинк становится слишком хрупким, что может привести к поломке.
Физические свойства
- Атомный номер: 30.
- Атомная масса: 65,37.
- Атомный объем: 9,15
- Плотность: 7,133 г/см 3 .
- Температура, необходимая для плавления: 419,5 C о .
- Температура кипения: 906 C о .
- Поверхностная энергия: 105 мДж/м 2 .
- Удельная электропроводность: 16,2*10 -6 См/м.
- Молярная теплоемкость: 25,4 Дж/(К*моль).
- Молярный объем: 9,2 см 3 /моль.
Цинк обладает слабыми механическими свойствами, при нормальной температуре легко ломается и крошится, но при температуре 100 C о -150 C о становится довольно тягучим и легко поддается деформации: куется, раскатывается в листы. Простая вода для металла безопасна, а кислоты и щелочи легко разъедают. Из-за этого цинк в чистом виде для изготовления деталей не применяют, только сплавы.
Применение цинка Для защиты металлов от коррозии
Чистый цинк используется для защиты металлов от коррозии. Основу покрывают тонкой пленкой. Этот процесс называется металлизацией.
В автомобильной отрасли
Сплавы на цинковой основе используют для оформления декора автомобильного салона, в производстве ручек дверей, замков, зеркал и корпусов стеклоочистителей.
В автомобильные покрышки добавляют окись цинка, которая повышает качество резины.
В батарейках, аккумуляторах и других химических источниках тока цинк используется как материал для отрицательного электрода. В производстве электромобилей применяются цинк-воздушные аккумуляторы, которые обладают высокой удельной энергоемкостью.
В производстве ювелирных украшений
Ювелиры добавляют цинк в сплавы на основе золота. В итоге они легко поддаются ковке и становятся пластичными — прочно соединяют мелкие детали изделия между собой.
Металл также осветляет ювелирные изделия, поэтому его часто используют в изготовлении белого золота.
В медицине
Окись цинка применяется в медицине как антисептическое средство. Окись добавляют в мази и другие составы для заживления ран.
Благодаря своим свойствам, цинк широко применяется в различных областях промышленности. Металл пользуется спросом из-за относительно низкой цены и хороших физических свойств.
Химические свойства
 Внешняя электронная конфигурация одного атома цинка можно записать как 3 d 10 4 s 2 . Металл активен и является энергичным восстановителем. При температуре в 100 C о на открытом воздухе покрывается пленкой, состоящей из основных карбонатов, и сильно тускнеет. При воздействии углекислого газа и повышенной влажности элемент начинает разрушаться. В кислородной или обычной среде при сильном нагревании цинк сгорает, образуя голубоватое пламя и белый дым, который состоит из оксида цинка. Огнеопасно воздействуют на цинк сухие элементы фтора, брома и хлора, но только при участии паров воды.
Внешняя электронная конфигурация одного атома цинка можно записать как 3 d 10 4 s 2 . Металл активен и является энергичным восстановителем. При температуре в 100 C о на открытом воздухе покрывается пленкой, состоящей из основных карбонатов, и сильно тускнеет. При воздействии углекислого газа и повышенной влажности элемент начинает разрушаться. В кислородной или обычной среде при сильном нагревании цинк сгорает, образуя голубоватое пламя и белый дым, который состоит из оксида цинка. Огнеопасно воздействуют на цинк сухие элементы фтора, брома и хлора, но только при участии паров воды.
При соединении металла и сильных минеральных кислот первый растворяется, особенно если смеси нагреть, в результате образуются соответствующие соли. Щелочи, расплавы и растворы окисляют вещество, в результате образуются цинкиты, растворимые в воде, и выделяется водород. Интенсивность воздействия кислот и щелочей зависит от наличия в цинке примесей. Чем более «чист» металл, тем слабее он взаимодействует из-за перенапряжения водорода.
.1 Способы переработки (обогащения) полезно го ископаемого
Технология переработки руд свинцово-цинковых
месторождений зависит от их минерального состава, степени окисления,
комплексности, текстуры и структуры, крупности зерен, степени взаимного
прорастания одних минералов другими, сопротивляемости руд дроблению и степени
шламообразования при их дроблении и измельчении.
Вследствие комплексного состава и относительно
невысоких содержаний ценных компонентов руды полиметаллических месторождений
подвергаются обогащению, преимущественно флотации.
В целях повышения содержаний свинца и цинка в рудах,
направляемых на флотацию, нередко применяется предварительное гравитационное
обогащение в тяжелых суспензиях, в результате чего отделяется 30-40 % пустой
породы с небольшими потерями свинца, цинка и меди в легкой фракции. Применение
гравитации позволяет вовлекать в промышленное освоение руды с относительно
низкими содержаниями металлов. Кроме того, для предобогащения руд возможно
применение радиометрической сортировки и радиометрической сепарации.
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
|
FI934550A0 * |
1993-10-14 | 1993-10-14 | Outokumpu Research Oy | Foerfarande och ugnkonstruktion foer anvaendning i processer i vilka laettflyktiga metaller produceras |
|
US5443614A * |
1994-07-28 | 1995-08-22 | Noranda, Inc. | Direct smelting or zinc concentrates and residues |
|
CN103602806B * |
2013-11-15 | 2014-12-31 | 吴鋆 | 一种高铟高铁锌精矿的冶炼方法 |
|
CN103740932B * |
2013-12-20 | 2015-08-26 | 中南大学 | 一种高铟高铁锌精矿的处理方法 |
|
WO2022140805A1 * |
2020-12-21 | 2022-06-30 | Tu Trinh Hong | Process for the production of zinc as zinc oxide or zinc metal directly from sulfide ores. |
|
WO2023154976A1 * |
2022-02-16 | 2023-08-24 | Glencore Technology Pty Limited | Method for processing zinc concentrates |
Info
- Publication number
- RU2091496C1
RU2091496C1
RU9393044975A
RU93044975A
RU2091496C1
RU 2091496 C1
RU2091496 C1
RU 2091496C1
RU 9393044975 A
RU9393044975 A
RU 9393044975A
RU 93044975 A
RU93044975 A
RU 93044975A
RU 2091496 C1
RU2091496 C1
RU 2091496C1
Authority
RU
Russia
Prior art keywords
zinc
copper
lead
matte
sulfide
Prior art date
1992-05-20
Application number
RU9393044975A
Other languages
English (en)
Other versions
RU93044975A
(ru
Inventor
Тапани Талонен Тимо
Йорма Ээрола Хеикки
Original Assignee
Оутокумпу Рисерч Ой
Priority date (The priority date is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the date listed.)
1992-05-20
Filing date
1993-05-12
Publication date
1997-09-27
Priority claimed from FI922301
external-priority
1993-05-12Application filed by Оутокумпу Рисерч Ой
filed
Critical
Оутокумпу Рисерч Ой
1996-11-20Publication of RU93044975A
publication
Critical
patent/RU93044975A/ru
1997-09-27Application granted
granted
Critical
1997-09-27Publication of RU2091496C1
publication
Critical
patent/RU2091496C1/ru
Производств цинка
Добыча металла
Цинк как самородный металл в природе не встречается. Добывается из полиметаллических руд, содержащих 1–4% металла в виде сульфида, а также меди, свинца, золота, серебра, висмута и кадмия. Руды обогащаются селективной флотацией и получаются цинковые концентраты (50–60% Zn).

Концентраты цинка обжигают в печах. Сульфид цинка переводится в оксид ZnO. При этом выделяется сернистый газ SO2, который используется в производстве серной кислоты.
Получение металла
Существуют два способа получения чистого цинка из оксида ZnO.
Самый древний метод — дистилляционный. Обожженный концентрированный состав подвергают термообработке, чтобы придать ему зернистость и газопроницаемость.
Затем концентрат восстанавливают коксом или углем при температуре 1200–1300 °C. В процессе образуются пары металла, которые конденсируют и разливают в изложницы. Жидкий металл отстаивают от железа и свинца при температуре 500 °C. Так достигается цинк чистотой 98,7%.
Иногда используется сложная и дорогая обработка цинка ректификацией — разделением смесей за счет обмена теплом между паром и жидкостью. Такая чистка позволяет получить металл чистотой 99,995% и извлечь кадмий.
Второй метод производства цинка — электролитический. Обожженный концентрат обрабатывается серной кислотой. Готовый сульфатный раствор очищается от примесей, после чего подвергается электролизу в свинцовых ваннах. Цинк дает осадок на алюминиевых катодах. Полученный металл удаляют с ванн и плавят в индукционных печах. После этого получается электролитный цинк чистотой 99,95%.
Литье металла
Горячий цинк — жидкий и текучий металл. Благодаря таким свойствам он легко заполняется в литейные формы.
Примеси влияют на величину натяжения поверхности цинка. Технологические свойства металла можно улучшить, добавив небольшое количество лития, магния, олова, кальция, свинца или висмута.
































