Использование в пищевой промышленности
Основной пищевой ингредиент — сахар
Сахароза — один из наиболее широко используемых ингредиентов в пищевой промышленности . Он составляет основу некоторых секторов, таких как кондитерская , кондитерская , производство джемов и напитков.
В фармацевтической промышленности он используется в качестве вспомогательного вещества.
Физико-химия
Сахароза хорошо растворяется в воде, и ее растворимость увеличивается с температурой. Он относительно стабилен, однако он может ферментировать (нежелательное явление в целом, за исключением алкогольных напитков) или гидролизоваться (превращаться, на языке кондитеров) в глюкозу и фруктозу , причем это явление можно контролировать.
При использовании в производстве напитков сахароза может быть инвертирована сама по себе во время термообработки. Кроме того, инвертный сахар более растворим, чем сахароза, поэтому в его присутствии он может действовать как удерживающий воду и предотвращать ее кристаллизацию.
Сахароза снижает активность воды в продуктах, которые ее содержат, что позволяет сохранить их.
Его также можно использовать в качестве вспомогательной текстуры из-за его качества слеживания .
Гранулометрия
Различные размеры кристаллов в зависимости от потребностей отрасли:
- кристаллический сахар;
- сахарная пудра ;
- сахарная пудра ;
- зерновой сахар.
Примечания и ссылки
- ↑ и
- ↑ и (in) на , по состоянию на 5 октября 2009 г.
- ↑ и (en) Уильям Дж. Колонна и Упасири Самаравира, Кирк-Отмерская энциклопедия химической технологии: Свойства сахарозы , т. 23, John Wiley & Sons., 4- е изд. , стр. 4.
- рассчитывается молекулярная масса от .
- ↑ и (en) Мохаммед Матлути и П. Райзер, Сахароза: свойства и применение , Springer,1995 г., 294 с. , стр. 107.
- (in) в банке данных по опасным веществам (по состоянию на 18 февраля 2010 г. ) .
- saccarose является орфографическим предложенным орфографическими поправками французов в 1990 году : .
- (in) CA Beevers TRR McDonald JH Робертсон и Ф. Стерн , « Кристаллическая структура сахарозы » , Acta Crystallographica , vol. 5,1952 г., стр. 689-690 .
- (in) RC Hynes и Y. Le Page , « Сахароза, удобный тест для определения абсолютных кристаллических структур » , Journal of Applied Crystallography , Vol. 24,1991 г., стр. 352-354 .
- ↑ и (ru) Питер М. Коллинз, Словарь углеводов , Бока-Ратон, CRC Press ,2005 г., 1282 с. ( ISBN 0-8493-3829-8 ) , стр. 538.
- (in) Словарь углеводов Питера М. Коллинза , Бока-Ратон, CRC Press ,2005 г., 1282 с. ( ISBN 0-8493-3829-8 ) , стр. 948.
- (in) М.А. Годшалл, на ,январь 2007(по состоянию на 7 ноября 2008 г. ) , стр. 12-20.
- (in) Словарь углеводов Питера М. Коллинза , Бока-Ратон, CRC Press ,2005 г., 1282 с. ( ISBN 0-8493-3829-8 ) , стр. 537.
- (in) Шмуэль Яннаи, Словарь пищевых соединений с компакт-диском: добавки, ароматизаторы и ингредиенты , Бока-Ратон, CRC Press , 2004 г., 1784 с. , стр. 1243–1244.
-
(in) RU Лемье и Г. Хубер , Химический синтез сахарозы , Журнал Американского химического общества , Vol. 75, п о 16,
Август 1953 г., стр. 4118-4118 . - (in) Нил Л. Пеннингтон и Чарльз У. Бейкер, Sugar, руководство пользователя по сахарозе , Springer,1990 г., 331 с. , стр. 49.
- ↑ и (ru) Дэвид Р. Лид, Справочник CRC по химии и физике , CRC Press ,2003 г., 84- е изд. , 2616 с. , 8 -81.
- (in) RS Shallenberger, Taste Chemistry , Лондон, Springer,1993 г., 613 с. , «Химическая природа, психология и физиология вкуса» , с. 5-46.
-
(in) Джон Э. Ланн , Метаболизм сахарозы , eLS ,
декабрь 2008. - РЕГЛАМЕНТ (ЕС) N о 916/2014 Комиссии22 августа 2014 г.утверждение основного вещества «сахароза» в соответствии с Регламентом (ЕС) п о 1107/2009 Европейского парламента и Совета в отношении размещения на рынке средств защиты растений, а также о внесении изменений в приложение к реализации Регламента (ЕС) п О 540/2011 Комиссии
Что такое биосинтез углеводов?
Определение
Биосинтез углеводов – это процесс синтеза или производства углеводных соединений в живых организмах. Углеводы являются одной из основных классов органических соединений и выполняют различные функции в организме, такие как поставка энергии, хранение энергии, структурная поддержка и участие в клеточных сигнальных процессах.
Биосинтез углеводов происходит в различных клеточных органеллах, включая хлоропласты у растений и митохондрии у животных. Процесс начинается с превращения простых прекурсоров, таких как глюкоза или другие моносахариды, в более сложные углеводные соединения.
Главный путь биосинтеза углеводов называется гликолизом. В ходе гликолиза глюкоза разлагается на молекулы пируватов, при этом образуется небольшое количество энергии. Пируваты могут далее претерпевать различные метаболические пути, включая глюконеогенез и гликогенез, которые приводят к синтезу и накоплению углеводов.
Углеводы также могут синтезироваться в ходе фотосинтеза у растений, где они образуются из воды и углекислого газа при участии света и хлорофилла.
Биосинтез углеводов является важным процессом для жизнедеятельности организмов, поскольку углеводы являются основным источником энергии и необходимы для многих биохимических процессов.
Как осуществляется биосинтез углеводов?
Биосинтез крахмала начинается с глюкозо-6-фосфата. Донором глюкозы служит сахароза.
На первой стадии синтеза глюкозо-6-фосфат превращается в глюкозо-1-фосфат.
На второй стадии образуется донор активированной глюкозы:
АТФ + глюкозо-1-фосфат АДФГ + пирофосфат
Для большинства растений донором активированной глюкозы является АДФГ.
На третьей стадии синтеза осуществляется перенос активированной глюкозы от АДФГ на акцептор.
Акцептором, или затравкой, в данном случае служит небольшая молекула полисахарида, состоящая иногда всего лишь из 3-4 остатков глюкозы, соединенных гликозидными связями. Реакцию катализирует фермент из подкласса гликозилтрансфераз.
В результате затравка постепенно удлиняется. Так происходит биосинтез амилозы. Затем часть амилозы используется для биосинтеза амилопектина.
Синтез амилопектина подразделяется на синтез неразветвленной и разветвленной частей. Неразветвленная часть образуется аналогично амилозе.
В синтезе разветвленной части участвует ветвящий фермент (Q-фермент), который отщепляет от неразветвленной цепочки фрагмент, построенный из остатков глюкозы, соединенных а-1,4-гликозидными связями, и переносит его к шестому атому углерода одного из остатков глюкозы неразветвленной части амилопектина.
ИЗОФЕРМЕНТНЫЙ СОСТАВ И ПРОФИЛЬ ЭКСПРЕССИИ ГЕНОВ САХАРОЗОСИНТАЗЫ У ДРЕВЕСНЫХ РАСТЕНИЙ
У большинства растений присутствует несколько изоформ СС, кодируемых мультигенным
семейством и отличающихся по своим биологическим функциям и кинетическим характеристикам.
Гены, кодирующие изоформы СС, различаются по нуклеотидной последовательности и профилям
экспрессии .
Наиболее изучены изоформы СС у травянистых растений . Исследования функции генов СС проведены, в основном, на модельном растении Arabidopsis, у которого выделено 6 изоформ СС (Sus1-6), объединенных в 3 пары на основании филогенетического анализа . В большей степени изучены изоформы фермента, кодируемые генами Sus1 и Sus2, участвующие в синтезе крахмала в запасающих тканях . Участие СС в синтезе целлюлозы на примере травянистых растений обсуждается в обзоре
Haigler с соавторами []. У трансгенных растений с пониженной активностью СС наблюдается снижение целлюлозы
в клеточной стенке, по сравнению с растениями дикого типа.
Работ, посвященных изучению изоформ СС у древесных растений, очень мало, в основном,
такие исследования проводятся на растениях рода Populus. Результаты структурного анализа показали наличие у растений тополя семи генов, кодирующих
разные изоформы СС, которые располагаются в 4 (из 19) хромосомах []. Высокая идентичность по аминокислотной (АК) последовательности у изоформ и нуклеотидной
последовательности кодирующих их генов, найдена между Sus1 и Sus2, Sus4 и Sus5, Sus6 и Sus7. Ген Sus3 выделяют в отдельную группу. Показано, что изоформы СС тополя SS1 и SS2 на 80.9–85.7%
идентичны данным изоформам картофеля, томата, Arabidopsis по АК последовательности, и, в меньшей степени, изоформам однодольных (пшеница, кукуруза)
– на 74.1–80.0% []. В базе данных национального центра биотехнологической информации США (National
Center for Biotechnological Information, NCBI) имеется информация по 3 генам (Sus1, Sus2, Sus3), кодирующим СС для видов рода Betula – B. luminifera, B. platyphylla. В 2017 году был секвенирован геном березы повислой, и проведен геномный анализ популяций
B. pendula, а также семи других представителей семейства Betulaceae [].
В исследованиях по изучению экспрессии генов сахарозосинтазного семейства показано,
что изменение уровня экспрессии генов СС влияет на содержание целлюлозы в ксилеме
древесных растений в большей степени, чем травянистых , а также определяет свойства древесины .
Анаболизм прокариот и биосинтез углеводов
Основные компоненты прокариотной клетки состоят из органических веществ-полисахаридов, белков, нуклеиновых кислот, липидов, большинство из которых (исключая липиды) являются полимерами.
Образованию полимеров предшествует биосинтез мономеров, их составляющих. На процессы биосинтеза мономеров и реакции их полимеризации расходуется большая часть энергии, получаемой клеткой в процессах катаболизма.
Прокариоты способны синтезировать моно-, олиго-, и полисахариды, а также и другие соединения, в состав которых входят углеводы.
Для прокариот-автотрофов исходным продуктом для синтеза углеводов является СО2.
Фотосинтезирующие автотрофные микроорганизмы фиксируют СО2 и осуществляют биосинтез углеводов также, как растения при фотосинтезе, через восстановительный пентозофосфатный цикл, или цикл Кальвина. Из клеток автотрофных прокариот выделены два специфических фермента этого цикла:
Фосфорибулокиназа, фосфорилирующая рибулозо-5-фосфат при участии АТФ в рибулозо-1,5-дифосфат, выступающий далее акцептором СО2.
Рибулозодифосфаткарбоксилаза, катализирующая реакцию фиксации СО2 рибулозо-1,5-дифосфатом с образованием двух молекул
3-фосфоглицериновой кислоты. 3-ФГК подвергается различным превращениям до получения глюкозы.
Подобным образом фиксируют СО2 и ведут синтез углеводов хемосинтезирующие автотрофные микроорганизмы.
Но они используют энергию АТФ, получаемую клеткой в результате реакций окисления неорганических веществ субстрата.
Моносахариды, образовавшиеся в результате фиксации СО2, используются на синтез олиго- и полисахаридов.
Источники сахарозы
В природе сахароза присутствует в большом количестве растений, в частности в их корнях , плодах и нектаре , где она используется для хранения энергии, возникающей в результате фотосинтеза . Многие млекопитающие , птицы , насекомые и бактерии питаются сахарозой растений, а некоторые делают ее своей основной пищей. В этом отношении пчелы играют особую роль в рационе человека , производя из нектара мед, потребляемый во всех частях света. Однако сахар в меде в подавляющем большинстве состоит из глюкозы и фруктозы , и лишь со следами сахарозы.
По мере созревания плодов уровень сахарозы обычно очень быстро увеличивается, но некоторые фрукты почти не содержат сахарозы. Это, например, случай виноград , вишни , черники ( черника ), ежевика , инжир , гранаты , помидоры , авокадо , лимоны и лайм .
Что такое биосинтез белка?
Определение
Биосинтез белка – это процесс, в ходе которого происходит синтез или производство белковых молекул в клетках организмов. Белки являются основными структурными и функциональными компонентами клеток и выполняют различные задачи, такие как поддержка структуры тканей, участие в химических реакциях, передача сигналов и многое другое.
Процесс биосинтеза белка происходит на основе генетической информации, содержащейся в ДНК. Вначале, информация из ДНК транскрибируется в молекулу РНК (рибонуклеиновую кислоту) в процессе транскрипции. Затем, молекула РНК переносится в рибосомы — клеточные органеллы, где происходит процесс трансляции, при котором кодированная информация из РНК используется для синтеза белка.
В ходе трансляции, специальные молекулы РНК, называемые транспортными РНК (тРНК), доставляют аминокислоты — строительные блоки белков — к рибосомам. Рибосомы, в свою очередь, связывают аминокислоты в определенном порядке, основываясь на последовательности кодона на молекуле РНК. Этот процесс продолжается до тех пор, пока не будет собрана полная молекула белка.
Биосинтез белка является сложным и регулируемым процессом, и его правильное функционирование существенно для нормального развития и функционирования клеток и организмов в целом.
Что такое липиды?
Липиды имеют очень большое значение в метаболизме клетки. Все липиды — ϶ᴛᴏ органические водонерастворимые соединения, присутствующие во всех живых клетках.
Необходимо отметить, что по своим функциям липиды разделяются на три группы:
— структурные и рецепторные липиды клеточных мембран
— энергетическое ʼʼдепоʼʼ клеток и организмов
— витамины и гормоны ʼʼлипиднойʼʼ группы
Основу липидов составляют жирные кислоты (насыщенные и ненасыщенные) и органический спирт – глицерол.
Основную массу жирных кислот мы получаем из пищи (животной и растительной). Животные жиры — ϶ᴛᴏ смесь насыщенных (40-60%) и ненасыщенных (30-50%) жирных кислот. Растительные жиры наиболее богаты (75-90%) ненасыщенными жирными кислотами и наиболее полезны для нашего организма.
Основная масса жиров используется для энергетического обмена, расщепляясь специальными ферментами – липазами и фосфолипазами.
В результате получаются жирные кислоты и глицерин, которые в дальнейшем используются в реакциях гликолиза и цикла Кребса.С точки зрения образования молекул АТФ — жиры составляют основу энергетического запаса животных и человека.
Эукариотическая клетка получает жиры с пищей, хотя сама может синтезировать большинство жирных кислот (за исключением двух незаменимых– линолевой и линоленовой).
Синтез начинается в цитоплазме клеток с помощью сложного комплекса ферментов и заканчивается в митохондриях или гладком эндоплазматическом ретикулуме.
Исходным продуктом для синтеза большинства липидов (жиров, стероидов, фосфолипидов) служит ʼʼуниверсальнаяʼʼ молекула – ацетил-Коэнзим А (активированная уксусная кислота), являющаяся промежуточным продуктом большинства реакций катаболизма в клетке.
Жиры есть в любой клетке, но особенно много их в специальных жировых клетках – адипоцитах, образующих жировую ткань. Контролируется жировой обмен в организме специальным гормонами гипофиза, а также инсулином и адреналином.
Углеводы (моносахариды, дисахариды, полисахариды) являются важнейшими соединениями для реакций энергетического обмена.
В результате распада углеводов клетка получает большую часть энергии и промежуточные соединения для синтеза других органических соединений (белков, жиров, нуклеиновых кислот).
Основную массу сахаров клетка и организм получает извне – из пищи, но может синтезировать глюкозу и гликоген из неуглеводных соединений.
Субстратами для разного вида углеводного синтеза выступают молекулы молочной кислоты (лактат) и пировиноградной кислоты (пируват), аминокислоты и глицерин. Эти реакции идут в цитоплазме при участии целого комплекса ферментов – глюкозо-фосфотаз. Для всех реакций синтеза требуется энергия – синтез 1 молекулы глюкозы требует 6 молекул АТФ!
Основной объём собственного синтеза глюкозы протекает в клетках печени и почек, но не идет в сердце, мозге и мышцах (там нет необходимых ферментов).
По этой причине нарушения углеводного обмена в первую очередь сказываются на работе этих органов. Углеводный обмен контролируется группой гормонов: гормонами гипофиза, глюкокортикостероидными гормонами надпочечников, инсулином и глюкагоном поджелудочной железы. Нарушения гормонального баланса углеводного обмена приводит к развитию диабета.
Мы кратко рассмотрели основные части пластического обмена.
Синтез — сахароза
Синтез сахарозы в растительных клетках, особенно в фото-синтезирующих клетках, осуществляется очень легко и непрерывно. В связи с этим также непрерывно должна идти и регенерация УТФ, необходимой для синтеза. Этот процесс и наблюдается в растениях.
Синтез сахарозы сопровождается еще одной реакцией — расщеплением неорганического пирофосфата с образованием орто-фосфата.
Синтез сахарозы, как было показано Лелуаром и другими авторами , при помощи УДФГ может протекать двумя путями.
Интенсивность синтеза сахарозы в клубнях составляет около 1 мкМ на 1 г в 1 час или около 0 06 мкМ на 1 мг белка. Сопоставление с литературными данными показывает, что синтез сахарозы в клубнях протекает слабее, чем во многих растениях.
Как происходит синтез сахарозы.
В последние годы показан синтез сахарозы через уридиндифос-фатглюкозу ( УДФГ) во многих растениях — зародышах пшеницы, сахарном тростнике, проростках и листьях сахарной свеклы, ростках картофеля, семенах гороха.
Проблема химии Сахаров — синтез сахарозы — была разрешена лишь в 1953 г. ( Р. У. Лемье); при нагревании 1 2-ангидро — 3 4 6-триацетил-х — В-глюкозы с 1 3 4 6-тетраацетил — В-фруктофуранозой образуется октаацетат сахарозы, из которого этот дисахарид был выделен гидролизом.
Под влиянием цинка повышаются синтез сахарозы, крахмала, общее содержание углеводов — и белковых веществ. Применение цинковых удобрений увеличивает содержание аскорбиновой кислоты, сухого вещества и хлорофилла в листьях кукурузы.
В качестве акцептора при синтезе сахарозы может выступать фруктозо-6 — фосфат, в котором фруктоза находится в фуранозной форме. Под действием фосфатазы синтезированный сахарид превращается в сахарозу.
Этот метод, приводящий к синтезу высших сахароз из низших, уже рассмотрен на стр.
При недостатке калия в растениях ослабляется синтез сахарозы, крахмала и жиров, повышается содержание моносахаридов. При внесении же калийных удобрений биосинтез и накопление в растениях сахарозы, крахмала и жиров резко усиливаются.
Уридиндифосфатглюкоза UDPG является промежуточным соединением в синтезе сахарозы в растениях. Этот кофермент реагирует с о-фруктозо-б-фосфатом с образованием уридин-дифосфата ( UDP) и сахарозофосфата. Последний затем гидроли-зуется до сахарозы.
В настоящее время не вызывает сомнений факт синтеза сахарозы как основного продукта, получаемого в зеленых листьях растений в процессе усвоения ими углекислого газа из воздуха под действием солнечного света.
Авторы считают, что промежуточными веществами в синтезе сахарозы являются глюкоза-1 — фосфат и фруктоза-6 — фос-фат. Фруктоза-фосфат образуется раньше глюкозы-фосфата. Это подтверждается тем, что фруктозная часть сахарозы, образовавшейся за 30 сек. Chlorella, имеет примерно в два раза большую удельную радиоактивность по сравнению с глюкозной частью.
В настоящее время метод Руффа весьма широко используется при синтезе меченых сахароз.
Обмен гликогена
Реакции пентозофосфатного пути протекают в цитозоле.
Образование АТФ.
По другому вторичному пути катаболизма глюкозы в животных тканях образуются два специализированных продукта: D-глюконат, важная роль которого связана с обезвреживанием и выведением из организма чужеродных органических веществ, и L-аскорбиновая кислота (витамин С).
Взаимосвязь пентозного пути и гликолиза.
В печени происходит превращение избытка углеводов в нерастворимый полимер – гликоген.
Эта резервная форма глюкозы может составлять одну десятую всей массы печени. При голодании запас гликогена почти полностью истощается.
Обмен гликогена включает в себя 2 процесса: гликогенез или синтез гликогена и гликогенолиз или распад гликогена.
Гликогенез – синтез гликогена — ϶ᴛᴏ анаболический процесс, требующий затраты энергии в форме как АТФ, так и уридинтрифосфата (УТФ).
Исходным источником для синтеза гликогена является глю, d под действием глюкокиназы превращается в глю-6-фосфат.
Глю-6-ф занимает ключевое положение как общий промежуточный продукт ряда процессов углеводного обмена: он способен к обратимому превращению в пируват путем гликолиза или глюконеогенеза, а также к необратимому – в пентозы в ходе фосфоглюконатного пути. Глю-6-ф может обратимо превращаться в гликоген.
Источником глю при синтезе гликогена является УДФ-глю, d образуется из глюкозо-1-ф и УТФ:
Глю-1-ф + УТФ УДФ=глю + Н4Р2О7
На следующей стадии происходит перенос остатка глю с УДФ-глю на затравку гликогена с помощью гликогенсинтетазы:
УДФ-глю + (глю)nУДФ +(глю)n+1
Гликогенсинтетаза катализирует образование только -1,4-гликозидных связей. ʼʼВетвящийʼʼ фермент образует -1-6 гликозидные S (точки ветвления).
Гликогенолиз – распад гликогена идет путем фосфоролиза.
Гликолиз, пентозофосфатный путь, гликогенолиз — ϶ᴛᴏ катаболические пути, которые сходятся в цикле лимонной кислоты, чтобы передать свои богатые энергией электроны в дыхательную цепь.
Перемещаясь по дыхательной цепи к кислороду, эти электроны поставляют энергию для синтеза АТФ. Теперь нам предстоит рассмотреть анаболические пути.
На этих путях химическая энергия в форме АТФ и НАДФН используется для синтеза клеточных компонентов из простых предшественников.
Биосинтез полисахаридов
Биосинтез полисахаридов осуществляется путем трансгликозилирования (переноса остатков моносахаридов на конец растущей цепи полисахарида) и всегда сопровождается затратой энергии.
Прокариоты-гетеротрофы способны синтезировать углеводы из С2 и С3-соединений, используя при этом реакции гликолитического пути, идущие в обратном направлении.
Все гетеротрофные микроорганизмы, помимо усвоения органических углерод содержащих веществ, фиксируют углекислый газ и используют его в реакциях анаболизма и катаболизма.
Включение СО2 в вещества клетки у гетеротрофных микроорганизмов происходит в реакциях карбоксилирования.
В большинстве случаев акцепторами СО2 выступают органические кислоты, например реакции карбоксилирования пировиноградной кислоты с образованием щавелевоуксусной (ЩУК) или яблочной кислот:
СН3-СО-СООН + СО2 +АТФ пируваткарбоксилаза НООС-СН2-СО-СООН + +АДФ+Фн.
СН3-СО-СООН +СО2 +НАД(Ф)Н малатдегидрогеназа НООС-СН2-СНОН-СООН +НАД(Ф)+
УЧАСТИЕ САХАРОЗОСИНТАЗЫ В ФОРМИРОВАНИИ КЛЕТОЧНЫХ СТЕНОК КСИЛЕМЫ
Образование ксилемы (ксилогенез) у древесных растений происходит поэтапно и включает
деление камбиальных инициалей и ксилемных производных камбия, их рост и дифференциацию,
отложение вторичной клеточной стенки, лигнификацию клеточных оболочек и программированную
клеточную смерть .
В ходе ксилогенеза активное включение сахарозосинтазы в метаболизм клеток происходит
на стадии отложения вторичной клеточной стенки, данный этап является очень важным,
поскольку именно вторичные клеточные стенки имеют наибольшую массовую долю в древесине
[]. Участие СС в формировании клеточной стенки обеспечивается за счет образования комплексов
из ее мембраносвязанной формы с целлюлозосинтазой . Такая ассоциация дает возможность прямого поступления УДФ-глюкозы, образующейся
в ходе сахарозосинтазного расщепления сахарозы, к месту синтеза клеточной стенки.
УДФ-глюкоза служит субстратом для синтеза β‑(1 → 4)-глюкановых цепей целлюлозы ().
Рис. 4.
Схематическое изображение целлюлозосинтазного комплекса. Сахарозосинтаза, связанная
с плазматической мембраной клетки, входит в состав целлюлозосинтазного комплекса.
Образующаяся УДФ-глюкоза поступает напрямую к месту синтеза β-(1→4)-глюкановых цепей
целлюлозы.

В последнее время появляется все больше работ, в которых участие СС в синтезе целлюлозы
демонстрируется с помощью данных молекулярно-генетического анализа. Среди древесных
растений такие исследования активно ведутся на тополе. На трансгенных растениях тополя
показано, что высокий уровень экспрессии генов сахарозосинтазного семейства коррелирует
с активным утолщением вторичных клеточных стенок ксилемы и приводит к увеличению прочности
древесины . На взрослых деревьях тополя (Populus tremula) [], сеянцах его гибридных линий P. alba × P. gradidentata [], P. deltoides × P. trichocarpa [], P. tremula × P. tremuloides [], а также на взрослых растениях двух форм березы повислой (B. pendula var. pendula и var. carelica) [] выявлена корреляция между уровнем экспрессии генов, кодирующих СС, и количеством
содержащейся в древесине целлюлозы. Участие СС в образовании древесины показано на
гибридных линиях тополя P. alba × gradidentata [], P. deltoids × trichocarpa [] и P. tremula × tremuloides []. Выявлено влияние СС на содержание целлюлозы, гемицеллюлоз, лигнина на единицу объема
древесины. Снижение экспрессии генов, кодирующих СС, приводит к изменению хемотипа
клеточной стенки (в частности, в составе лигнина происходит увеличение соотношения
сирингильные/гваяцильные единицы) [].
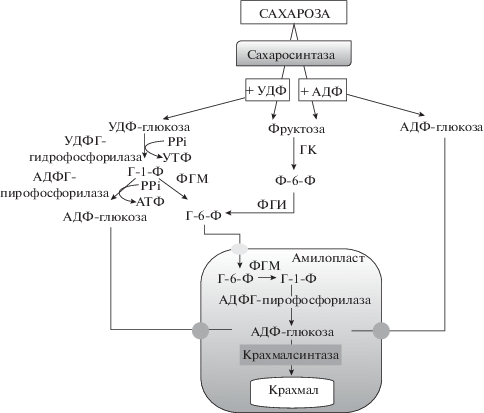
РОЛЬ САХАРОЗОСИНТАЗЫ В БИОСИНТЕЗЕ КРАХМАЛА
В литературе имеются многочисленные данные об участие СС в биосинтезе крахмала . Схематическое изображение возможных путей биосинтеза крахмала представлено на . УДФ-глюкоза, образованная при расщеплении сахарозы СС, переводится в глюкозо-1-фосфат
(Г‑1-Ф) в реакции, катализируемой УДФГ-пирофосфорилазой. Из Г-1-Ф образуется (1) глюкозо-6-фосфат
(Г-6-Ф) под действием фосфоглюкомутазы (этот путь, в большей степени, встречается
у двудольных растений) или (2) АДФ-глюкоза в реакции, катализируемой АДФГ-пирофосфорилазой
(этот путь протекает при развитии семян однодольных растений). Г-6-Ф и АДФ-глюкоза,
в свою очередь, транспортируются в амилопласты. АДФ-глюкоза непосредственно используется
на синтез крахмала в реакции, катализируемой крахмалсинтазой, а Г-6-Ф преобразуется
в Г-1-Ф и переводится в АДФ-глюкозу при участии АДФГ-пирофосфорилазы (). Путь образования крахмала из УДФ-глюкозы считается приоритетным в акцепторных тканях
растений , и УДФ является преимущественным субстратом для сахарозосинтазной реакции . Показано, что АДФ также может вступать в катализируемую СС реакцию. В результате
такой реакции образуется АДФ-глюкоза, транспортируемая к месту синтеза крахмала в
амилопласты ().
Рис. 6.
Участие сахарозосинтазы в синтезе крахмала. ГК – гексокиназа, ФГМ – фосфоглюкомутаза,
ФГИ – фосфоглюкоизомераза, Ф-6-Ф – фруктозо-6-фосфат, Г-6-Ф – глюкозо-6-фосфат, Г-1-Ф
– глюкозо-1-фосфат, АДФ – аденозиндифосфат, АТФ–аденозинтрифосфат, УДФ – уридиндифосфат, УТФ – уридинтрифосфат, PPi – пирофосфат.
Работы, выполненные на травянистых растениях, показывают корреляцию активности СС
с накоплением крахмала в запасающих тканях и органах . У древесных растений основная функция СС в тканях ствола в период камбиального
роста – участие в синтезе компонентов клеточных стенок ксилемы. На разновозрастных
деревьях березы повислой показано, что в этот период на фоне высокой активности СС
запасание крахмала происходит слабо [], а продукты метаболизации сахарозы расходуются преимущественно на синтез целлюлозы
[]. В условиях временного торможения камбиальной деятельности погодными условиями происходило
снижение активности СС в ксилеме. При этом возрастала утилизация сахарозы во флоэме,
и на фоне повышения активности СС происходило значительное накопление крахмала в проводящей
флоэме []. У растений карельской березы в местах формирования аномалий содержание крахмала
было намного выше, и при этом наблюдается корреляция активности СС с накоплением крахмала,
как во флоэме, так и в ксилеме, что, вероятно, связано с увеличением числа паренхимных
клеток в составе узорчатой древесины . Таким образом, в тканях ствола древесных растений в период камбиального роста СС
может принимать участие в синтезе крахмала (1) во флоэме при появлении избыточных
количеств сахарозы в проводящей флоэме и (2) в ксилеме при дифференцировке камбиальных
производных в паренхимные клетки (живые клетки лучевой и аксиальной паренхимы) вместо
прозенхимных клеток (сосуды, волокна).
В заключение следует отметить, что спектр функций, выполняемых СС в растениях, очень
широк. Очевидно, что в акцепторных тканях древесных растений физиологически наиболее
значимым является участие данного фермента в синтезе компонентов клеточных стенок
сосудов и волокон, составляющих основную часть древесной биомассы. На разных видах
древесных растений показано, что СС обеспечивает приоритетный путь метаболизации сахарозы
в ходе ксилогенеза. Регуляция активности СС, в значительной степени, осуществляется
на уровне транскрипции, и уровень экспрессии кодирующих ее генов неодинаков в ксилеме
древесных растений, различающихся по структурному составу древесины. В свою очередь,
изоферментный состав СС и уровень транскрипции генов, кодирующих определенные изоформы,
очень сильно варьирует в зависимости от условий внешней среды, стадии онтогенеза и
типа растительной ткани. При воздействии определенных факторов и в зависимости от
условий клеточной среды СС, помимо ее участия в формировании вторичных клеточных стенок,
может включаться также в биосинтез крахмала и каллозы. Продукты сахарозосинтазного
расщепления сахарозы могут расходоваться в процессах дыхания и общем метаболизме клетки.
Данные о деятельности СС в акцепторных органах древесных растений могут быть использованы
для изучения продуктивности и поиска путей управления ксилогенезом.
Работа выполнена при финансовой поддержке грантов Российского фонда фундаментальных
исследований № 16-04-100639_ р_а и № 16-04-01191_а, средств федерального бюджета на
выполнение государственного задания ИЛ КарНЦ РАН.


















![Синтез сахарозы и полисахаридов [1983 гэлстон а., дэвис п., сэттер р. - жизнь зеленого растения]](http://lesniepolyani.ru/wp-content/uploads/c/5/e/c5e856ba6cae01676fe73c774071dc71.png)











