Урок 17. Получение кислорода – HIMI4KA
 Архив уроков › Химия 8 класс
Архив уроков › Химия 8 класс
В уроке 17 «Получение кислорода» из курса «Химия для чайников» выясним, как получают кислород в лабораторных условиях; узнаем, что такое катализатор, и как растения влияют на производство кислорода на нашей планете.
Наиболее важным для человека и других живых организмов веществом, входящим в состав воздуха, является кислород
Большие количества кислорода используются в промышленности, поэтому важно знать, как можно его получать
Получение кислорода в лабораторных условиях
В химической лаборатории кислород можно получать нагреванием некоторых сложных веществ, в состав которых входят атомы кислорода. К числу таких веществ относится вещество KMnO4, которое имеется в вашей домашней аптечке под названием «марганцовка».
Вы знакомы с простейшими приборами для получения газов. Если в один из таких приборов поместить немного порошка KMnO4 и нагреть, то будет выделяться кислород (рис. 76):
Кислород можно также получить разложением пероксида водорода H2O2. Для этого в пробирку с H2O2 следует добавить очень небольшое количество особого вещества — катализатора — и закрыть пробирку пробкой с газоотводной трубкой (рис. 77).
Для данной реакции катализатором является вещество, формула которого MnO2. При этом протекает следующая химическая реакция:
Обратите внимание на то, что ни в левой, ни в правой частях уравнения формулы катализатора нет. Его формулу принято записывать в уравнении реакции над знаком равенства
Для чего же добавляется катализатор? Процесс разложения H2O2 при комнатных условиях протекает очень медленно. Поэтому для получения заметных количеств кислорода необходимо много времени.
Однако эту реакцию можно резко ускорить путем прибавления катализатора.
Катализатор — это вещество, которое ускоряет химическую реакцию, но само в ней не расходуется.
Именно потому, что катализатор не расходуется в реакции, мы не записываем его формулу ни в одной из частей уравнения реакции.
При этом протекает следующая химическая реакция:
Кислород в природе
Огромное количество газообразного кислорода содержится в атмосфере, растворено в водах морей и океанов. Кислород необходим всем живым организмам для дыхания. Без кислорода невозможно было бы получать энергию за счет сжигания различных видов топлива. На эти нужды ежегодно расходуется примерно 2% атмосферного кислорода.
Откуда берется кислород на Земле и почему его количество остается примерно постоянным, несмотря на такой расход? Единственным источником кислорода на нашей планете являются зеленые растения, производящие его под действием солнечного света в процессе фотосинтеза.
Это очень сложный процесс, включающий много стадий. В результате фотосинтеза в зеленых частях растений углекислый газ и вода превращаются в глюкозу C6H12O6 и кислород.
Суммарное уравнение реакций, протекающих в процессе фотосинтеза, можно представить следующим образом:
Установлено, что примерно одну десятую часть (11%) производимого зелеными растениями кислорода дают наземные растения, а остальные девять десятых (89%) — водные растения.
Получение кислорода и азота из воздуха
Огромные запасы кислорода в атмосфере позволяют получать и использовать его в различных производствах. В промышленных условиях кислород, азот и некоторые другие газы (аргон, неон) получают из воздуха.
Для этого воздух сначала превращают в жидкость (рис. 79) путем охлаждения до такой низкой температуры, при которой все его компоненты переходят в жидкое агрегатное состояние.
https://youtube.com/watch?v=bMDdeYmAD5k
Затем эту жидкость медленно нагревают, в результате чего при разных температурах происходит последовательное выкипание (т. е. переход в газообразное состояние) веществ, которые содержатся в воздухе. Собирая выкипающие при разных температурах газы, по отдельности получают азот, кислород и другие вещества.
Краткие выводы урока:
- В лабораторных условиях кислород получают разложением некоторых сложных веществ, в состав которых входят атомы кислорода.
- Катализатор — вещество, которое ускоряет протекание химической реакции, но само при этом не расходуется.
- Источником кислорода на нашей планете являются зеленые растения, в которых протекает процесс фотосинтеза.
- В промышленности кислород получают из воздуха.
Надеюсь урок 17 «Получение кислорода» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
Реферат патента 2017 года Электролизер для получения водорода и кислорода из воды
Изобретение относится к электролизеру для получения водорода и кислорода из воды, состоящему из корпуса с размещенными в нем катодом в виде полого цилиндра из пористого гидрофобизированного материала и анодом в виде трубы из металла, находящегося между ними сепаратора в виде газозапорной мембраны, с образованием катодной газовой полости между внешней стенкой катода и внутренней стенкой корпуса, анодной полости внутри анода, с нанесенными на поверхность анода и поверхность катода катализатором. Электролизер характеризуется тем, что анод выполнен из перфорированного металлического листа с присоединенной по его наружной поверхности металлической сеткой с нанесенным на нее катализатором, катод изготовлен из пористого гидрофобизированного материала с нанесенным на его наружную поверхность со стороны водородной полости катализатором, а с внутренней стороны с присоединенной к нему сеткой с нанесенным на нее катализатором, сепаратор состоит из газозапорной мембраны из пористого гидрофильного материала, окруженной с обеих сторон одним или несколькими слоями сепарационного материала, герметизация полости водорода относительно полости кислорода осуществляется при сборке электролизера как за счет фланцев, выполненных из электроизоляционного материала и имеющих кольцевые канавки с прокладками для создания уплотнения по торцам катода в местах соприкосновения с фланцами, так и за счет обжатия при сборке электролизера верхнего и нижнего концов сепаратора, выступающих за пределы анода и сеток, присоединенных к катоду и аноду, между внешними концевыми конусообразными поверхностями соответствующих фланцев и соответствующими внутренними концевыми конусообразными поверхностями катода. Использование предлагаемого устройства позволяет минимизировать энергетические затраты на собственные нужды и, как следствие, повысить КПД заявляемого электролизера, повысить надежность работы электролизера и чистоту вырабатываемых газов. 8 з.п. ф-лы, 3 ил.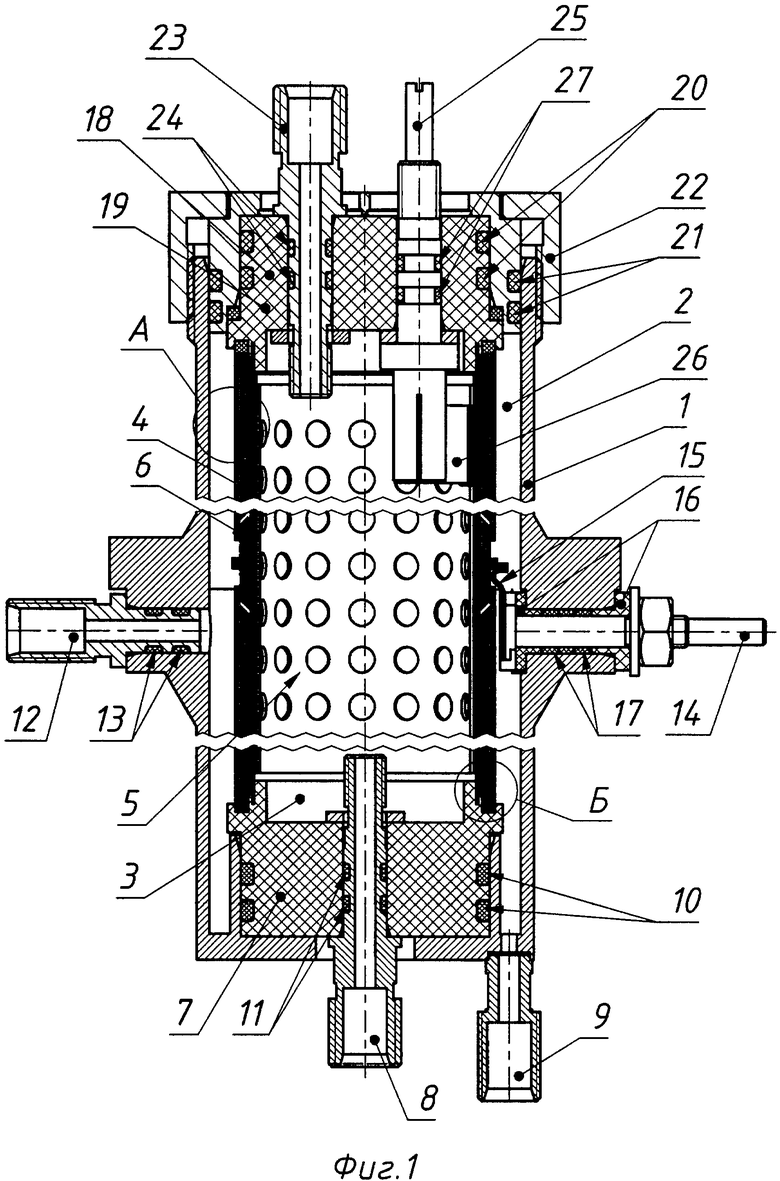
Выгодно ли получать водород в домашних условиях
Ответ на данный вопрос зависит от сферы применения кислородно-водородной смеси. Все чертежи и схемы, публикуемые различными интернет-ресурсами, рассчитаны на выделение газа HHO для следующих целей:
- использовать hydrogen в качестве топлива для автомобилей;
- бездымно сжигать водород в отопительных котлах и печах;
- применять для газосварочных работ.
Главная проблема, перечеркивающая все преимущества водородного топлива: затраты электричества на выделение чистого вещества превышают количество энергии, получаемое от его сжигания. Что бы ни утверждали приверженцы утопичных теорий, максимальный КПД электролизера достигает 50%. Это значит, что на 1 кВт полученной теплоты затрачивается 2 кВт электроэнергии. Выгода – нулевая, даже отрицательная.

Важная справочная информация. Удельная теплота сгорания водорода втрое выше, чем у метана, но – по массе. Если сравнивать их по объему, то при сжигании 1 м³ гидрогена выделится всего 3.6 кВт тепловой энергии против 11 кВт у метана. Ведь водород – легчайший химический элемент.
Теперь рассмотрим гремучий газ, полученный электролизом в самодельном водородном генераторе, как топливо для вышеперечисленных нужд:
- Конечная цена установки, низкая производительность и КПД делает крайне невыгодным сжигание водорода для отопления частного дома. Чем «наматывать» счетчик электролизером, проще поставить любой из электрокотлов – ТЭНовый, индукционный либо электродный.
- Чтобы заменить 1 л бензина для автомобиля, потребуется 4766 литров чистого водорода или 7150 л гремучего газа, треть которого составляет кислород. Самый завравшийся изобретатель в интернете еще не сделал электролизер, способный обеспечить подобную производительность.
- Газосварочный аппарат, сжигающий hydrogen, компактнее и легче баллонов с ацетиленом, пропаном и кислородом. Плюс температура пламени до 3000 °С позволяет работать с любыми металлами, стоимость получения горючего здесь особой роли не играет.
Для справки. Чтобы сжигать гидроген в отопительном котле, придется основательно переработать конструкцию, поскольку водородная горелка способна расплавить любую сталь.
https://youtube.com/watch?v=C5rSrR-6N1g%3Ffeature%3Doembed
Как получить кислород из воды формула
Получение О₂ из воды в процессе электролиза. Этот эксперимент получится, если в воде содержится определенное количество солей. Поэтому он будет протекать интенсивнее, если в обычную воду добавить поваренную соль. 1. Взять два куска проволоки, подсоединить к разным клеммам батарейки (лучше использовать 9-вольтовую типа «Крона»). 2. Опустить оба конца проволоки в солевой раствор. А в другой (перевернутой) пробирке соберется получаемый в результате газ — кислород. Его будет много: из 10 грамм марганцовки можно сделать примерно 1 литр газа. Проверить, есть ли в колбе кислород, можно, поместив в пробирку горящую спичку. Яркое свечение пламени укажет на присутствие О₂. Share.
В этой статье вы узнаете, как расщепить воду на кислород и водород с помощью электролиза. Шаги. 1. Заполните обычный стеклянный стакан (диаметром около 7,5 см) водопроводной водой примерно на 3/4. 2. Растворите в воде столовую ложку поваренной соли. Соль повысит электропроводность воды. Графитовый стержень проще и безопаснее получить из простого карандаша. Заточите два карандаша с обоих концов и подсоедините к ним проволоку. Погрузите карандаши в воду. Образование пузырьков газа на графитовых стержнях будет интенсивней. Запишите ваши наблюдения. За небольшую цену вы можете приобрести медные контакты, покрытые платиной.
Как получить из воды кислород
Составьте уравнение реакции получения кислорода из воды и 8/9 кислорода. соответственно выйдет 40 г. кислорода и 5 в водорода Как из водорода и кислорода получить ВОДУ?

В этой статье вы узнаете, как расщепить воду на кислород и водород с помощью Для получения значительного количества водорода (и кислорода) Не найдено: формула.
Разложение воды на водород и кислород часть 1
https://youtube.com/watch?v=tHfNCDw-Kr4
ПОХОЖИЕ МАТЕРИАЛЫ:
12.05.2018 в 01:35 Башиктуева Людмила:Я думаю, что Вы не правы. Я уверен. Давайте обсудим.
25.05.2018 в 11:50 Джерыкина Татьяна:По моему мнению, это — заблуждение.
О водородной ячейке Мейера
Если вы сделали и испытали вышеописанную конструкцию, то по горению пламени на конце иглы наверняка заметили, что производительность установки чрезвычайно низкая. Чтобы получить больше гремучего газа, нужно изготовить более серьезное устройство, называемое ячейкой Стэнли Мейера в честь изобретателя.
Принцип действия ячейки тоже основан на электролизе, только анод и катод выполнены в виде трубок, вставляющихся одна в другую. Напряжение подается от генератора импульсов через две резонансные катушки, что позволяет снизить потребляемый ток и увеличить производительность водородного генератора. Электронная схема устройства представлена на рисунке:
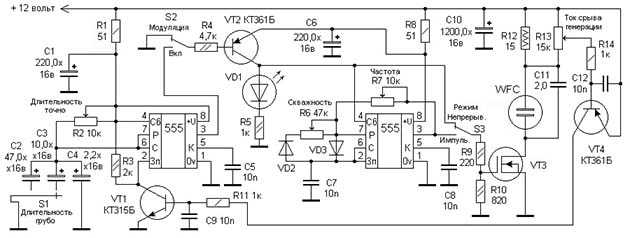
Примечание. Подробно о работе схемы рассказывается на ресурсе http://www.meanders.ru/meiers8.shtml.
Для изготовления ячейки Мейера потребуется:
- цилиндрический корпус из пластмассы или оргстекла, умельцы нередко используют водопроводный фильтр с крышкой и патрубками;
- трубки из нержавеющей стали диаметром 15 и 20 мм длиной 97 мм;
- провода, изоляторы.

Нержавеющие трубки крепятся к основанию из диэлектрика, к ним припаиваются провода, подключаемые к генератору. Ячейка состоит из 9 или 11 трубок, помещенных в пластиковый либо плексигласовый корпус, как показано на фото.

Под ячейку Мейера можно приспособить готовый пластиковый корпус от обычного водопроводного фильтра
Соединение элементов производится по всем известной в интернете схеме, куда входит электронный блок, ячейка Мейера и гидрозатвор (техническое название – бабблер). В целях безопасности система снабжена датчиками критического давления и уровня воды. По отзывам домашних умельцев, подобная водородная установка потребляет ток порядка 1 ампера при напряжении 12 В и обладает достаточной производительностью, хотя точные цифры отсутствуют.
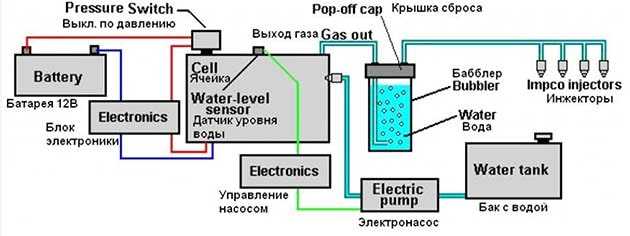
Принципиальная схема включения электролизера
Что такое способ получения кислорода из воды?
Способ получения кислорода из воды называется электролиз воды. Это процесс, в котором с помощью электрического тока разлагается вода на кислород и водород.
Для проведения электролиза воды необходимы следующие компоненты:
- Вода
- Электролит
- Две электроды
- Источник постоянного тока
Электролиз воды основан на применении закона Фарадея, согласно которому масса вещества, которое проходит через электролизер, пропорциональна количеству электричества, прошедшего через него.
В процессе электролиза вода разлагается на кислород и водород. Отрицательно заряженный электрод (катод) собирает водород, а положительно заряженный электрод (анод) собирает кислород. Полученный кислород можно использовать в различных областях, включая медицину, промышленность и научные исследования.
Электролиз воды — это эффективный способ получения кислорода из воды, который является одним из основных способов его производства.
Применение кислорода
Помимо того, что все живые существам в природе, за исключением немногих микроорганизмов, при дыхании потребляют кислород, он широко применяется во многих отраслях промышленности: металлургической, химической, машиностроении, авиации, ракетостроении и даже в медицине.
В химической промышленности его применяет:
- при получении ацетилена из природного газа (метана);
- при производстве кислот (азотной, серной);
- для газификации твердого топлива;
- для производства аммиака, формальдегида и метанола.
В металлургии его используют:
- при получении цветных металлов из руд;
- при выплавке чугуна в доменных печах;
- при выплавке стали в мартеновских и электрических печах;
- кислородно-конверторной выплавке стали.
В медицинских целях больным, у которых нарушена нормальная деятельность органов дыхания или кровообращения, искусственно увеличивают содержание O2 в воздухе или дают дышать непродолжительное время чистым O2. Медицинский кислород, выпускаемый ГОСТ 5583, особенно тщательно очищают от всех примесей.
Применение кислорода в сварке
Сам по себе O2 является негорючим газом, но из-за свойства активно поддерживать горение и увеличения интенсивности (интенсификации) горения газов и жидкого топлива его используют в ракетных энергетических установках и во всех процессах газопламенной обработки. В таких процессах газопламенной обработки, как газовая сварка, поверхностная закалка высокая температура пламени достигается путем сжигания горючих газов в O2, а при газовой резке благодаря ему происходит окисление и сгорание разрезаемого металла.
При полуавтоматической сварке (MIG/MAG) кислород O2 используют как компонент защитных газовых смесей с аргоном (Ar) или углекислым газом (CO2).
Кислород добавляют в аргон при полуавтоматической сварке легированных сталей для обеспечения устойчивости горения дуги и струйного переноса расплавленного металла в сварочную ванну. Дело в том, что как поверхностно активный элемент он уменьшает поверхностное натяжение жидкого металла, способствуя образованию на конце электрода более мелких капель.
При сварке низколегированных и низкоуглеродистых сталей полуавтоматом O2 добавляют в углекислый газ для обеспечения глубокого проплавления и хорошего формирования сварного шва, а также для уменьшения разбрызгивания.
Чаще всего кислород используют в газообразном виде, а в виде жидкости используют только при его хранении и транспортировке от завода-изготовителя до потребителей.
Возможные проблемы и решения
При использовании способа получения кислорода из воды могут возникнуть следующие проблемы:
- Недостаточное количество воды. Если количество воды недостаточно, то процесс получения кислорода может быть затруднен или невозможен. Решение: увеличить количество воды или применить альтернативные способы получения кислорода.
- Низкая концентрация кислорода в воде. Если концентрация кислорода в воде низкая, то процесс получения кислорода может занимать больше времени и требовать дополнительных ресурсов. Решение: использовать специальные методы для повышения концентрации кислорода в воде.
- Загрязнения в воде. Наличие загрязнений в воде может негативно повлиять на процесс получения кислорода и качество полученного продукта. Решение: применять очистку воды перед процессом получения кислорода или использовать специальные системы фильтрации.
В целом, способ получения кислорода из воды позволяет обеспечить необходимые ресурсы для поддержания жизнедеятельности и снятия проблем, связанных с недостатком кислорода. Однако, для успешной реализации этого способа, необходимо учитывать возможные проблемы и применять соответствующие решения для их устранения.
Опасные последствия
Кислород является незаменимым элементом для существования живых организмов. Вода, в свою очередь, является одним из основных источников кислорода. Но какой способ получения кислорода из воды называется?
Один из способов получения кислорода из воды называется электролиз. Этот процесс основывается на разложении воды на кислород и водород при помощи электрического тока. При этом кислород выделяется на положительном электроде, водород — на отрицательном. Электролиз воды широко применяется в промышленности, а также в науке и медицине.
Однако, несмотря на полезность и широкое применение электролиза воды, его неправильное применение может иметь опасные последствия. При неправильной эксплуатации электролизера или нарушении технологических процессов возможно образование взрывоподобных смесей из водорода и кислорода, что может привести к авариям и несчастным случаям.
Поэтому для безопасного получения кислорода из воды необходимо строго соблюдать все инструкции и правила, предусмотренные для данного процесса, а также использовать специальное оборудование и инструменты
При правильной эксплуатации и соблюдении всех мер предосторожности, получение кислорода из воды является безопасным и эффективным процессом
Разработка безопасных методов
Кислород называется одним из наиболее важных газов, необходимых для жизни. Он используется в медицине, промышленности и сфере бытового потребления. Один из способов получения кислорода — из воды.
Как известно, вода состоит из молекул, каждая из которых содержит атомы кислорода и водорода. При помощи специальных технологий и устройств возможно разделить эти молекулы и получить кислород в чистом виде.
Одним из методов получения кислорода из воды является электролиз. Этот метод основан на использовании электрического тока, который проходит через раствор воды. При этом происходит разложение молекулы воды на кислород и водород. Кислород выделяется на одном полюсе, а водород — на другом.
Другим способом получения кислорода из воды является химический метод. При этом используется процесс разложения воды на молекулы кислорода и водорода при наличии определенных химических веществ или катализаторов.
Важно отметить, что разработка безопасных методов получения кислорода из воды является приоритетной задачей
При работе с высокочувствительными и взрывоопасными веществами необходимо соблюдать строгие меры предосторожности. Кроме того, применение новейших технологий и материалов позволяет повысить эффективность и безопасность процесса получения кислорода
Кроме того, применение новейших технологий и материалов позволяет повысить эффективность и безопасность процесса получения кислорода.
Общее представление о различных методах получения кислорода из воды позволяет находить новые пути и технологии для улучшения эффективности, безопасности и экологической чистоты процесса. Это важный вклад в развитие науки и техники, а также в обеспечение кислородом человечества.
История
Устройство, изобретенное Иоганном Вильгельмом Риттером для разработки электролиза воды.
В 1789 году Ян Рудольф Дейман и Адриан Паэтс ван Троствейк использовали электростатическую машину для производства электричества, которое разряжалось на золотых электродах в лейденской банке с водой. В 1800 году Алессандро Вольта изобрел гальваническую батарею , а несколько недель спустя английские ученые Уильям Николсон и Энтони Карлайл использовали ее для электролиза воды. В 1806 году Хамфри Дэви сообщил о результатах обширных экспериментов по электролизу дистиллированной воды, сделав вывод, что азотная кислота образуется на аноде из растворенного атмосферного азота. Он использовал высоковольтную батарею и инертные электроды и сосуды, такие как конусы золотых электродов, которые дублировались как сосуды, перекрытые влажным асбестом. Когда Зеноб Грамм изобрел машину Грамма в 1869 году, электролиз воды стал дешевым методом производства водорода. Метод промышленного синтеза водорода и кислорода электролизом был разработан Дмитрием Лачиновым в 1888 году.
Обычная батарейка расщепляет воду на кислород и водород!
В отличие от традиционного топлива, которое выделяет вредные выхлопные газы, загрязняющие атмосферу и приводящие к изменению климатических условий, водородное топливо абсолютно безвредно для окружающей среды.
Почему все транспортные средства не используют водород в качестве топлива?
До сих пор экологически чистый процесс получения водорода требовал большого количества драгоценных металлов, что значительно повышает стоимость водородного топлива, особенно в сравнении с традиционным.
Путем химического взаимодействия атомов водорода с атомами кислорода, находящегося в воздухе, водородное топливо вырабатывает достаточно энергии для двигателя автомобиля, а «выхлопами» такого мотора становится чистая вода. Однако сегодня практически каждый «чистый» двигатель, который работает на водородном топливе, использует водород, полученный с помощью природного газа – процесс, экологическая чистота которого находится под сомнением.
Как получить «чистый» водород?
С помощью электрических потоков воду можно разделить на атомы кислорода и водорода. Этот процесс требует большого количества дорогих металлов, таких как платина или иридий, – они хорошо проводят электричество и не портятся, находясь в воде долгое время.
Процесс расщепления молекулы воды на атомы водорода и кислорода называется электролизом и проходит следующим образом: два электрода опускаются в воду, по ним проводится ток, под действием которого атомы водорода стремятся к отрицательно заряженному катоду, а атомы кислорода к положительно заряженному аноду.
Новый прорыв
Ученые из Стэндфордского университета провели уникальный эксперимент, в результате которого совершили процесс электролиза с помощью стандартных никелевых электродов под рекордно низким напряжением — обычная батарейка в 1.5 Вольт.
По данным ученых, конструкция электродов из никеля и его оксида позволила процессу успешно завершиться под таким низким напряжением. До этого никому не удавалось совершить подобное. Новая технология в промышленных масштабах поможет производителям водородного топлива значительно сэкономить на электричестве и проводниках. Сейчас ученые работают над тем, как увеличить продолжительность работы никелевых проводников в воде.
ГЕНЕРАТОР ВОДОРОДА своими руками. Производит водород отдельно от кислорода.

Бонусы новым игрокам в Crossout: https://xo.pub/ognennoetv.Мощная установка для раздельного получения газов выделяющихся при электролизе воды: водорода и кислорода..В этот раз получилось собрать чистый кислород..Ты можешь поддержать мой канал финансово, все собранные средства я трачу на покупку нового оборудования и приборов. Карта Сбербанка 5469 3800 4423 1909.QIWI https://qiwi.com/qiwi.com/n/OGNENNOETV.Яндекс Деньги 410011465014776.Webmoney R374674113509 Z583934586764 E800928670495 K366735448132.Bitcoin 1HBZPijMwdtajciZLpDLJ5M6PxPwRMVWnD.Litecoin LYG2WBwJWYBtp8ojLwTkscr8wFjesLppty.—Подпишись на мой инстаграм, там я выкладываю разные интересные штуки. https://www.instagram.com/i_polynkov/.—Телеграм-канал для экстренной связи. https://t.me/ognennoetv.—Музыка предоставлена epidemicsound.com.В лаборатории Огненного ТВ можно проводить химические и физические эксперименты, создавать необычные механизмы, воплощать самые безумные идеи и проверять на прочность всем известные мифы..Если ты изобретатель и естествоиспытатель по духу, если тебе тоже интересна химия, физика, механика, интересны эксперименты с электричеством магнитными волнами, то присоединяйся к нашему сообществу, подписывайся на Огненное ТВ!Огненное ТВ это научные эксперименты, техническое творчество и познавательный контент.
Электролиз воды в домашних условиях
Для получения чистого кислорода и водорода используют химические лаборатории, однако и в домашних условиях такую реакции произвести более чем возможно. Понадобится:
- источник тока (любой гальванический элемент)
- емкость с возможностью разделения
- электроды (графитовые, золотые или платиновые пластины)
- вода (дистиллированная, вода из-под крана или бутилированная не подойдет)
Следует понимать, что источник тока должен обладать небольшим потенциалом (около 9 Вольт), иначе есть возможность получить удар электрическим током при несоблюдении техники безопасности. Подключаем клеммы источника тока с электродам, заливаем в емкость воды (можно добавить сильную щелочь или разбавленную серную кислоту). Теперь можно запустить ток и наблюдать образование кислорода и водорода на аноде и катоде соответственно.

В данной статье вы узнали, что такое электролиз воды, его свойства и вид реакции (эндотермическая). С помощью электролиза воды можно в домашних условиях получить молекулы чистого кислорода и водорода посредством проведения электрического тока через раствор дистиллированной воды по электродам (катоду и аноду). Вода диссоциирует на катионы водорода и анионы кислорода. Положительные ионы движутся к катоду, отрицательные ионы – к аноду. Для ускорения протекания реакции (катализа) можно добавить в дистиллированную воду сильный электролит, который не вступит в конфликт с ионами воды.
Создание опытного образца
Чтобы вы поняли, с чем имеете дело, для начала предлагаем собрать простейший генератор по производству водорода с минимальными затратами. Конструкция самодельной установки изображена на схеме.
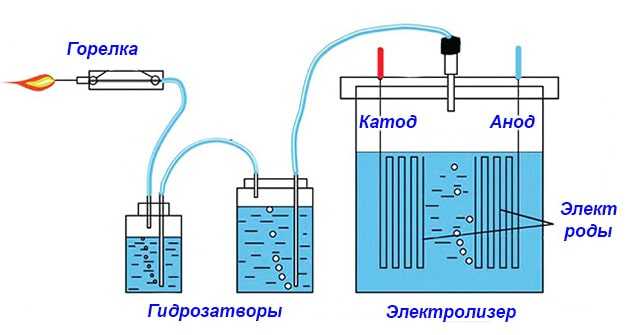
Из чего состоит примитивный электролизер:
- реактор – стеклянная либо пластиковая емкость с толстыми стенками;
- металлические электроды, погружаемые в реактор с водой и подключенные к источнику электропитания;
- второй резервуар играет роль водяного затвора;
- трубки для отвода газа HHO.
Важный момент. Электролитическая водородная установка работает только от постоянного тока. Поэтому в качестве источника питания применяйте сетевой адаптер, автомобильное зарядное устройство или аккумулятор. Электрогенератор переменного тока не подойдет.
Принцип работы электролизера следующий:
- К двум электродам, погруженным в воду, подводится напряжение, желательно от регулируемого источника. Для улучшения реакции в емкость добавляется немного щелочи либо кислоты (в домашних условиях – обычной соли).
- В результате реакции электролиза со стороны катода, подключенного к «минусовой» клемме, станет выделяться водород, а возле анода – кислород.
- Смешиваясь, оба газа по трубке поступают в гидрозатвор, выполняющий 2 функции: отделение водяного пара и недопущение вспышки в реакторе.
- Из второй емкости гремучий газ ННО подается на горелку, где сжигается с образованием воды.
Чтобы своими руками сделать показанную на схеме конструкцию генератора, потребуется 2 стеклянных бутылки с широкими горлышками и крышками, медицинская капельница и 2 десятка саморезов. Полный набор материалов продемонстрирован на фото.

Из специальных инструментов потребуется клеевой пистолет для герметизации пластиковых крышек. Порядок изготовления простой:
- Плоские деревянные палочки скрутите саморезами, располагая их концами в разные стороны. Спаяйте головки шурупов между собой и подсоедините провода – получите будущие электроды.
- Проделайте отверстие в крышке, просуньте туда разрезанный корпус капельницы и провода, затем герметизируйте с 2 сторон клеевым пистолетом.
- Поместите электроды в бутылку и завинтите крышку.
- Во второй крышке просверлите 2 отверстия, вставьте трубки капельниц и накрутите на бутылку, заполненную обычной водой.
Для запуска генератора водорода налейте в реактор подсоленную воду и включите источник питания. Начало реакции ознаменуется появлением пузырьков газа в обеих емкостях. Отрегулируйте напряжение до оптимального значения и подожгите газ Брауна, выходящий из иглы капельницы.
https://youtube.com/watch?v=-WR7VLmWuaw%3Ffeature%3Doembed























