Различия между нитрификацией и денитрификацией — нитрификация против денитрификации
| База для сравнения | нитрификация | денитрификация |
| Определение | Нитрификация – это биологический процесс, который включает окисление аммиака до нитрита с последующим превращением нитрита в нитрат. | Денитрификация — это биологический процесс, который восстанавливает нитраты до нитритов. За этим следует преобразование нитрита в газообразный азот, что обычно приводит к удалению газообразного азота в воздух. |
| реакция | Общая реакция нитрификацииNH4+ – №2– – №3– | Общая реакция денитрификации: 2 NO3- + 10 e- + 12 H+ – N2 + 6 H2O |
| Шаги | Нитрификация представляет собой процесс, состоящий из двух реакций. | Процесс денитрификации происходит через серию полуреакций. |
| Обработка | Нитрификация – это метод химических реакций, вызывающих окисление. | Денитрификация — это процесс, который состоит из реакции восстановления. |
| Азотный цикл | Нитрификация является следующим шагом в круговороте азота. | Денитрификация является последней стадией азотного цикла. |
| Предполагает | Нитрификация – это процесс превращения восстанавливаемых соединений азота в окисленную форму. | Денитрификация — это процесс преобразования соединений азота, которые были окислены, в восстановленные версии. |
| Конечный продукт | Конечным продуктом нитрификации будет нитрат (NO3 –). | Продукт, который образуется при денитрификации, представляет собой либо закись азота (NO2), либо газообразный азот (N2). |
| Подложка | Первичным или исходным соединением для процесса нитрификации является аммиак. | Основными соединениями или субстратами для денитрификации являются нитраты, а также нитриты. |
| Концентрация кислорода | Различные микроорганизмы способны к нитрификации с большим количеством кислорода. | Различные микроорганизмы участвуют в денитрификации при низкой концентрации кислорода. |
| Вовлекаются микроорганизмы | Общие микроорганизмы, которые нитрифицируют, включают Нитросомонас, Нитрозококк. Нитробактер, Нитроспира, Нитрозопумилюс приморский так же как и сигнал Нитрозосфера винная. | Общие денитрифицирующие микроорганизмы включают Паракокк денитрификанс, ТЫоЬасШиз денитрификаторы, протеобактерии. |
| Питание | Большинство микробов, участвующих в нитрификации, являются химически автотрофными. | Большинство микробов, участвующих в нитрификации, являются гетеротрофными. |
| Требуемый рН | Нитрификация процветает в диапазоне рН от 6.5 до 8. | Денитрификация активно развивается в диапазоне рН от 7 до 9. |
| Температура | Процесс наиболее вероятен при температуре от 20 до 30 градусов по Цельсию. | Процесс обычно протекает при температуре от 26 до 38°С. |
| Ингибиторы | Некоторые ингибиторы, связанные с процессом нитрификации, включают серосодержащие соединения, а также N-гетероциклические вещества. | Некоторые ингибиторы, участвующие в денитрификации, включают ацетилен и цианид, а также некоторые пестициды, такие как вапам. |
| Значение | Нитрификация является жизненно важным процессом, который помогает поставлять нитраты растениям, которые являются источником азота. | Денитрификация является важным этапом, обеспечивающим циклическое перемещение азота из воздуха в почву, растения и обратно в атмосферу. Кроме того, это ключевой элемент в очистке сточных вод. |
Применение азота в сельском хозяйстве
Удобряя землю азотистыми соединениями из расчета — килограмм удобрений на гектар земли, можно повысить урожайность зерновых культур на несколько процентов. В сельском хозяйстве в виде урожая азот выносится в количестве 1 млн. тонн, при этом азотистых удобрений используется в два раза меньше. Несмотря на высокую рентабельность использования минеральных удобрений, потребности растений в этом веществе покрываются искусственным путем всего на 20-25%. Остальное его количество извлекается из грунта за счет биологической фиксации (естественные удобрения). Дальнейшее повышение урожайности будет зависеть лишь от рационального применения навоза, наращивания производства минеральных удобрений и эффективного использования «биологического» (произведенного микроорганизмами) связанного азота.

Почвенный покров региона и почва опытного участка
Почвенный покров республики Марий Эл представлен достаточно бедными по природе почвами, наиболее распространенными являются дерново-подзолистые почвы различного гранулометрического состава (Смирнов В.Н., 1968). Они занимают 552,2 тыс. га из 632, 2 тыс. га пашни, или 88,6 %. Серые и светло-серые лесные почвы занимают только 2,3 % (Шорин В.М., 1990). В зависимости от гранулометрического состава преобладают суглинистые почвы. Песчаные и супесчаные почвы занимают только 87,5 тыс. га, или 13,9 % пашни. Тяжелосуглинистые почвы занимают 64 тыс. га или 19,4 %, средне-суглинистые — 352,8 тыс. га или 56,6 %, а легкосуглинистые — 117,3 (18,8 %) тыс. га. Преобладающими являются дерново-подзолистые среднесуглини-стые малогумусные почвы.
Почвенный покров опытного участка представлен малогумусной дер-ново-среднеподзолистой среднесуглинистой почвой на опесчаненом бескарбонатном покровном среднем суглинке (Денисова Е. А., 2001).
Почвенный профиль резко дифференцирован на генетические горизонты. Верхние горизонты почвы обеднены илистой фракцией и содержат значительное количество крупной и средней пыли, опесчанены, малосвязны и бесструктурны. Нижние горизонты, наоборот, уплотнены, связны и трудно проницаемы для воздуха и воды. При выпадении осадков почва быстро заплывает и уплотняется, затрудняется воздухообмен и ослабляются микробиологические процессы (табл. 2). Исследования выполнены на кафедре агрохимии и земледелия Марийского государственного университета. Микрополевые, вегетационные и лабораторные исследования проводили на дерново-подзолистой среднесугли-нистой малогумусной почве. Модельный лабораторный опыт В модельных лабораторных опытах изучали влияние почвенных условий на микробоценоз, нитрифицирующую и аммонифицирующую способность почвы. В модельном опыте № 1 целью исследований являлось установление оптимальных условий для развития почвенных микроорганизмов. Изучаемые факторы: 1. температура почвы: -10; -5; 0; +15; +25; +35; +45 С ; 2. влажность почвы: 0; 5; 10; 15; 20; 25; 30 % к абс. сухой почве; 3. плотность почвы: 1,1; 1,2; 1,3; 1,4; 1,5; 1,6; 2 г/см . 4. органическое удобрение (навоз КРС) из расчета: 0; 40; 80; 120; 160; 200; 240 т/га. В качестве органического удобрения использовался навоз КРС с содержанием N — 0,45 %; Р205 — 0,21 %; К20 — 0,50 %.
В модельном опыте № 2 изучалось влияние реакции среды на нитрифицирующую и аммонифицирующую способность почвы. Дозы извести вносили из расчета: 0; 2,6 (0,5 Нг); 5,2 (1 Нг); 7,8 (1,5 Нг); 10,4 (2,0 Нг) т/га. В опыте использовалась известь второго сорта с содержанием СаС03 86 %. Фактически дозы навоза и извести были пересчитаны на 50 г сухой почвы. Повторность опытов — 4-6 кратная.
Для проведения исследований использовали дерново-подзолистую, среднесуглинистую малогумусную почву стационарного опыта кафедры. Минеральный азот (нитратный + аммонийный) определяли после двух недельного компостирования. Нитратный азот определяли потенциометриче-ским методом с использованием ионо-селективного электрода, а аммонийный — колориметрическим с реактивом Несслера.
Учет численности микроорганизмов проводили путем посева различных разведений на агаризованные питательные среды. Аммонифицирующие бактерии, использующие органические формы азота, учитывали на мясопеп-тонном агаре; нитрифицирующие бактерии — на агаризованной среде Скер-мана; целлюлозоразлагающие бактерии — на среде Гатчинсона с целлюлозным порошком; азотобактер — методом обрастания комочков почвы на среде Эшби (Сэги И., 1983; Методические рекомендации по оценке токсического действия пестицидов на микрофлору почвы, 1981; Некоторые новые методы количественного учета микроорганизмов и изучение их свойств, 1987).
Нитрифицирующую и аммонифицирующую способность почвы определяли после двухнедельного компостирования (Методические указания по определению нитрификационной способности почв, 1984; Александрова Л. Н., Найденова О. А., 1976).
Для моделирования почвенных условий почву уплотняли ручным прессом до расчетных значений. Необходимую влажность создавали высушиванием или увлажнением почвы. Высушивание почвы проводили в сушильном шкафу. Для получения различной влажности приливали к образцам почвы расчетное количество дистиллированной воды. Влияние температуры изучали путем помещения образцов в холодильные шкафы и термостаты, установленные на заданную температуру.
Круговорот серы
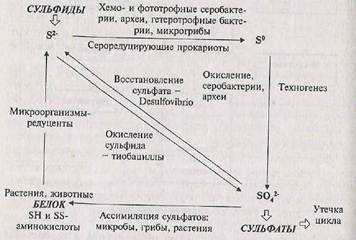
В глобальном круговороте серы (рис. ![]() кроме бактерий, грибов и растений, использующих сульфат природных вод и почвы для синтеза серосодержащих аминокислот, работают еще несколько групп специализированных бактерий, осуществляющих превращения в реакциях H2S о S SO4 и H2S SO4.
кроме бактерий, грибов и растений, использующих сульфат природных вод и почвы для синтеза серосодержащих аминокислот, работают еще несколько групп специализированных бактерий, осуществляющих превращения в реакциях H2S о S SO4 и H2S SO4.
Потребность биоты в сере относительно невелика (биофильность S»1), а природные резервуары серы огромны. Поэтому сера редко оказывается лимитирующим биогеном. Биотический круговорот серы включен в общий, в значительной своей части абиогенный, процесс постепенного превращения восстановленных форм серы (в основном сульфидных руд), сложившихся в восстановительной обстановке древней Земли, в окисленные формы. Эта тенденция существенно усиливается техногенезом.
Влияние аммиакокислотных бактерий на урожайность
Аммиакокислотные бактерии, также известные как нитрифицирующие бактерии, играют важную роль в почве и имеют значительное влияние на урожайность растений. Эти бактерии способны катализировать два ключевых процесса нитрификации — окисление аммония до нитрита и дальнейшее окисление нитрита до нитрата.
Нитрит является основным промежуточным продуктом в процессе нитрификации, и его распадподтипит растительной среды. Затем нитраты аммиакокислотные бактерии бактериями найти рози и заметить его вещества фитоткимикаты и прочие химические, водорастворимые растворы микроорганизмы в почве, подпитывая растения, и вносят важные питательные вещества в почву.
Вот несколько способов, которыми аммиакокислотные бактерии влияют на урожайность:
- Повышение доступности азота для растений. Бактерии нитрификации преобразуют аммоний в нитраты, которые легко усваиваются растениями через корни. Это увеличивает доступность азота для растений и стимулирует их рост.
- Улучшение структуры почвы. Нитрифицирующие бактерии производят полимеры, которые способствуют образованию агрегатов в почве и улучшают её структуру. Это способствует проникновению воды и воздуха в почву, а также уменьшает эрозию.
- Борьба с патогенными микроорганизмами. Некоторые аммиакокислотные бактерии производят антимикробные вещества, которые помогают сдерживать рост патогенных микроорганизмов в почве. Это способствует более здоровому росту растений и предотвращает развитие болезней.
- Улучшение питательной среды для растений. Нитраты, полученные в результате деятельности аммиакокислотных бактерий, являются важным источником азота для растений. Они способствуют синтезу белка, хлорофилла и других важных компонентов растений, что улучшает их рост и развитие.
Примерные данные урожайности (т/га) при использовании аммиакокислотных бактерий:
Вид культуры
Контроль
Без применения аммиакокислотных бактерий
С применением аммиакокислотных бактерий
Пшеница
3.5
4.1
4.8
Кукуруза
6.2
7.4
8.6
Помидоры
12.5
14.2
16.8
Эти данные показывают, что применение аммиакокислотных бактерий может значительно увеличить урожайность различных культур. Кроме того, они могут быть использованы как эффективная альтернатива химическим удобрениям, что способствует экологичному земледелию и сохранению природных ресурсов.
денитрификация
Денитрификация представляет собой биологическое превращение нитрата в азотные газы путем восстановления. Он всегда следует за нитрификацией я и последовательность реакции может быть представлена следующим образом:
НЕТ3– → НЕТ2– → НЕТ → N2O → N2
Процесс облегчается факультативными бактериями; это бактерии, которые не требуют наличия свободного кислорода для дыхания. Денитрифицирующие бактерии представляют собой гетеротрофные организмы, так как они нуждаются в органическом источнике пищи в форме углерода, чтобы выжить. Денитрификация может начинаться так же быстро, как и минуты после стимуляции процесса.
Денитрификация может нанести ущерб растениеводству, поскольку азот, питательный материал, необходимый для роста растений, теряется в атмосфере во время процесса. Тем не менее, это полезно для водных сред обитания, а также для очистки промышленных сточных вод или сточных вод, поскольку концентрация нитратов в воде снижается. я
Выщелачивание или сток из сельскохозяйственных культур в результате обработки удобрений может привести к избыточному количеству этого питательного вещества в конечном итоге в водоемах, где азотистые соединения оказывают различное вредное воздействие как на человека, так и на водную флору. IV
Аммиак является токсичным для видов рыб и стимулирует рост водорослей, снижает уровень кислорода в воде и приводит к эвтрофикации. Нитраты вызывают повреждение печени, рак и метгемоглобинемию (дефицит кислорода у младенцев), тогда как нитриты реагируют с органическими соединениями, называемыми аминами, с образованием канцерогенных нитрозаминов. б
Когда уровни кислорода в почвах или воде истощаются (аноксические условия), денитрифицирующие бактерии разрушают нитраты для использования в качестве источника кислорода. Это обычно происходит в заболоченных почвах, где уровни кислорода низки. Нитрат восстанавливается до закиси азота (N2O) и еще раз азотистым газом. Эти газовые пузырьки выходят в атмосферу. я
Газ, образованный денитрификаторами, зависит от условий в почве или воде, и какое микробное сообщество присутствует. Меньше кислорода, как правило, приводит к образованию большего количества образующегося азота, самого общего продукта денитрификации. Азотный газ образует основной компонент воздуха. Вторым наиболее распространенным продуктом является закись азота, парниковый газ, который также разрушает озоновый слой Земли. IV
Денитрифицирующие бактерии менее чувствительны к токсичным химикатам, чем нитрификаторы, и оптимально функционируют при рН между 7,0 и 8,5 и более теплыми температурами от 26 до 38 градусов Цельсия. Денитрификация происходит главным образом в верхнем слое почвы, где микробная активность является самой высокой.
Для денитрификаторов требуется достаточная концентрация нитратов и источник растворимого углерода; самые высокие показатели происходят при использовании метанола или уксусной кислоты. Органический углерод можно найти в навозе, компосте, покрытии культур и растительных остатках. я
Минимизация денитрификации в сельскохозяйственных культурах достигается за счет поддержания минимальной концентрации нитрата, необходимой для роста растений, например, использования удобрений с контролируемым высвобождением. Другим методом является ингибирование нитрификации, что снижает уровень нитрата, доступного для денитрификации.
Уровни денитрификации широко варьируются в пределах одного поля из-за многих факторов, таких как свойства почвы (включая агрегацию, макропоры и влажность) и изменения в распределении удобрений, органических веществ и культур.
Сообщалось, что типы азотных удобрений, а также методы применения влияют на денитрификацию. Например, удобрения с контролируемым высвобождением с покрытием, а также фертигация и широковещательные применения вызывают более низкие выбросы закиси азота, чем сухие гранулированные мочевины и концентрированные полосы. Более глубокое размещение азота также снижает эти выбросы.
Сухие периоды, сопровождаемые внезапным ливнем, часто являются спусковым крючком для денитрификации, которым можно управлять с помощью дренажных систем и подповерхностного капельного орошения. IV
Бактерии как основной двигатель круговорота азота
Азот содержится не только в атмосфере. Почти столько же его в гидросфере, земной коре и в мантии (примерно 4×10¹⁵ т). Геохимический круговорот требует, чтобы этот азот постоянно был включен в общий круговорот, поддерживая тем самым геохимическое стабильное состояние Земли.
Как известно, суть круговорота состоит в том, что элементы из атмосферы попадают в земную кору (разные ее слои) и в гидросферу, а из литосферы и гидросферы назад возвращаются в атмосферу. Исключение составляет только мантия, ее элементы извергаются в атмосферу с извержениями вулканов и уже туда не возвращаются. Но в мантии азота не так уж и много, поэтому его количество, извергаемое регулярно в атмосферу, не в состоянии изменить общий геохимический цикл.
Как уже говорилось, бактерии являются в азотном цикле единственным биогенным элементом:
- Клубеньковые и другие прокариоты поглощают молекулярный азот атмосферы и плодородных почв – верхнего слоя земной коры, после чего превращают его в органические соединения, которые могут усваиваться растениями.
- Растения поглощаются животными, в том числе и людьми, которые, погибая и разлагаясь, возвращают азотные соединения в воздух через процесс денитрификации, который также осуществляют бактерии, только уже представители другой группы – денитрификаторы.

Химия азота
Азот составляет 79 процентов воздуха, которым мы дышим. Поверхность 6 дюймов плодородной почвы прерий может содержать от 2 до 3 тонн азота на акр. Воздух над этим же акром будет содержать около 35 000 тонн инертного газообразного азота (N2). Большая часть азота, содержащегося в почве, происходит в виде газа N2, и почти весь азот в атмосфере — это газ N2. Этот инертный азот не может быть использован растением до тех пор, пока он не изменится на аммонийную (NH4 +) или нитратную (NO3 -).
Три важных метода замены газообразного азота (N2) на аммоний (NH4 +):
- Свободноживущие N2-фиксирующие бактерии
- N2-фиксирующие бактерии в клубеньках на корнях бобовых растений, и
- Заводы по производству азотных удобрений.
Другим важным методом преобразования N2 является молния. Когда молния мигает, газообразный азот в перегретом воздухе превращается в нитрат (NO3 -) и нитрит (NO2 -). Молния может составлять от 1 до 50 фунтов доступного для растений азота на акр в год.
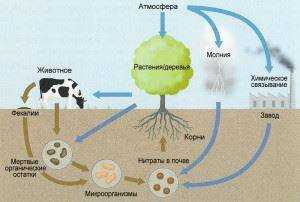
Хотя азот попадает в почву в нескольких химических формах, он в конечном итоге превращается в неорганический нитрат-ион (NO3 -). На рисунке 1 показано, что NO3 — может использоваться растениями, превращаться обратно в газообразный азот или вымываться вниз в почвенную воду.
Коммерческие удобрения, растительные остатки, навоз и сточные воды являются наиболее распространенными источниками добавления азота в почву. Нормы применения сильно различаются. Однократные нормы внесения могут составлять до 150 фунтов азотного эквивалента на акр для таких культур, как прибрежные бермуды. Однако такие высокие нормы внесения должны быть ограничены почвами с низким потенциалом эрозии и стока.
Азот в органических материалах (растительные остатки, навоз животных, сточные воды, органическое вещество почвы) присутствует в составе белков, аминокислот и других растительных и микробных материалов. Он становится доступным для растений только после разложения соединения почвенными микроорганизмами. Это называется «минерализация» (рис. 2). Первым этапом минерализации является «аммонификация». Аммоний (NH4 +), полученный в результате аммонификации, затем превращается в нитратный азот (NO3 — -N) путем «нитрификации» бактерий в почве с помощью процесса, называемого «нитрификация».
Места реакций аммонификации и нитрификации в азотном цикле показаны на рисунке 1. Положительно заряженный ион аммония (NH4 +), полученный аммонификацией или добавленный в почву в удобрениях, притягивается к отрицательно заряженным глинистым частицам в почве. Однако в большинстве не засушливых почв ион NH4 + быстро превращается в нитратный азот (NO3-N). Растущие растения поглощают большую часть своего азота в форме нитрата (NO3-).
Обычные источники неорганического азота включают аммиак (NH3), аммоний (NH4 +), амин (NH2 +) и нитрат (NO3 -). Большинство удобрений содержат или образуют NH4 +, который быстро превращается в NO3 — один раз в почве.
Аммонификация белков (минерализация азота)
Процесс выделения азота из аминокислот и превращение его в аммиачную форму называется аммонификацией. Микроорганизмы, вызывающие этот процесс, выделяют в окружающую среду протеолитические ферменты, под действием которых белки гидролизуются до аминокислот» Последние поступают в клетку и в ней дезаминируются с образованием аммиака, органических кислот и других продуктов.
Возбудителями процесса аммонификации являются аммонифицирующие или гнилостные бактерии. Их можно разделить на три группы по отношению к источникам кислорода:
1.Аэробы: Bacillus mycoides, Bacillus subtilis, Bacillus megatherium, Bacillus mesentericus.
Bacillus Mycoides – палочки 5-10 х 1,0-1,5 мкм, перитрихи, соединяются в цепочки, образуя жирные пленки на поверхности жидкой среды. Споры овальные, расположены эксцентрально (рис.33А).
Bacillus Subtilis — палочки короткие и тонкие, 3-5 х 0,6 мкм, нередко соединены в длинные нити. Споры овальные, расположены без строгой локализации (рис.33Г).
Bacillus Mesentericus -палочки тонкие, длинные и короткие, 3-10 х 0,5-0,6 мкм, одиночные или соединены в длинные нити. Споры овальные и продолговатые, бациллярного типа.
Bacillus Megatherium -клетки толстые до 2 мкм в диаметре, длина от 3 до 12 мкм. Содержимое клеток грубозернистое с большим количеством питательных веществ (жир, гликоген) (рис.33Б).
2. Анаэробы факультативные:
Proteus Vulgaris -палочки длиной от 1 до 20 мкм, перитрихи, спор не образуют, грамотрицательны (рис.33В) .
Escherichia СOli — кишечная палочка. Небольшие грамотри-цательные палочки, перитрихи, спор не образуют.
3.Анаэробы облигатные:
Bacillus Cadaveris, ВасIllus Putrificus — небольшие палочки до 5 мкм, образуют споры плектридиального типа. Выделяют трупные яды (кадаверин, путресцин).
|
А) Bacillus Mycoides |
Б) Bacillus Megatherium |
|
В) Proteus Vulgaris |
Г) Bacillus subtilis |
Рис. 33. Аммонификаторы белка (гнилостные бактерии)
Химизм процесса аммонификации:
1 этап — протеолиз белка – Проходит по схеме
NH2
Протеаза
Белок + N H2O аминокислоты (АК) : R—CH—COOH
2 этап – дезаминирование. — Бывает трех видов:
А)простое дезаминирование
NH2
R—CH—COOH R ═ CH—COOH + NH3
Б)окислительное дезаминирование:
NH2
R—CH—COOH + ½ O2 R—CO—COOH + NH3
В)восстановительное дезаминирование:
NH2
R—CH—COOH + H2 R—CH 2—COOH + NH3
Основные ферменты: протеазы, дезаминазы, трансаминазы.
Все аммонификаторы — гетеротрофы, аминогетеротрофы.
Значение процесса: перевод соединений азота в доступную для растений форму, подщелачивание кислых почв, порча пищевых продуктов. Многие аммонификаторы выделяют токсичные вещества (трупные яды – путресцин и кадаверин, а также ботулин – самый сильный пищевой яд).
Нахождение азота в природе
Большая часть азота в природе находится в свободном состоянии. Он является главной составной частью воздуха (объемная доля – 78,9%, массовая доля – 75,6%). Содержание азота в земной коре – 10*-2% масс.
Рис. 1. Формула азота.
Из соединений азота большое значение имеет натриевая (чилийская) селитра NaNO3, образующая большие пласты на побережье Тихого океана в Чили. Калиевая (индийская) селитра KNO3 обнаружена в ряде районов Индии. Нитрат кальция Ca(NO3)2*nH2O (n=0-4), также встречающийся в природе, называют «норвежской» селитрой.
Рис. 2. Норвежская селитра.
Незначительные количества азота преимущественно в виде солей азотной кислоты содержит почва. Азот также входит в состав белковых веществ и многих естественных органических соединений.
Нахождение азота в природе во многом связано с жизнедеятельностью бактерий и водорослей, так как многие микроорганизмы извлекают азот из разлагающихся отходов
Симбиотическая азотофиксация
Этот процесс осуществляется многими микроорганизмами в симбиозе как с бобовыми, так и с не бобовыми растениями.
Наиболее изучена фиксация азота бактериями рода Rhizobium в симбиозе с бобовыми растениями (рис.31). Известно 1300 видов бобовых, на корнях которых бактерии образуют клубеньки.
Представители рода Rhizobium — грамотрицательные бесспоровые палочки размером 0,5-0,9 х 1,2-3 мкм (рис.32а). Имеют жгутики (монотрихи или перитрихи). При старении теряют подвижность, накапливают жировые включения.

А б в г
Рис. 31. Клубеньки на корнях: А)люпина; б)люцерны; в)фасоли; г)вики.
В зрелой клубеньковой ткани бактериальные клетки превращаются в бактероиды: грушевидные, сферические или ветвистые образования (рис.32б). В таком виде клубеньковые бактерии наиболее энергично усваивают атмосферный азот. На питательных средах бактерии рода Rhizobium усваивают органические вещества (гетеротрофы), аэробы, могут использовать в качестве источника азота как минеральные, так и органические его формы, но не атмосферный азот. Способность к азотфиксации у ризобий сохраняется только в симбиозе с тканями бобовых растений.
Химизм симбиотической азотофиксации и ферменты те же, что и у свободноживущих микроорганизмов.
Микробная трансформация азота в биосфере Земли
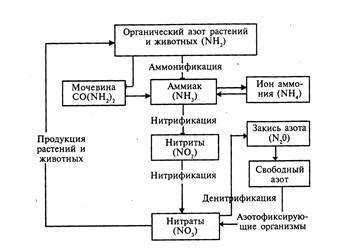
Запасы азота на планете Земля огромны. Основная масса его находится в атмосфере в молекулярной форме (N2). Эта форма азота химически инертна и может усваиваться лишь ограниченной группой микроорганизмов ─ бактериями, которые называются азотофиксаторами. Связанный ферментами бактерий азот называется биологическим и, циркулируя в биосфере, формирует биогеохимический цикл азота (рис.29). Круговорот азота происходит следующим образом: диазотрофы поглощают атмосферный азот и образуют аммиак, который служит исходным веществом для образования белков.
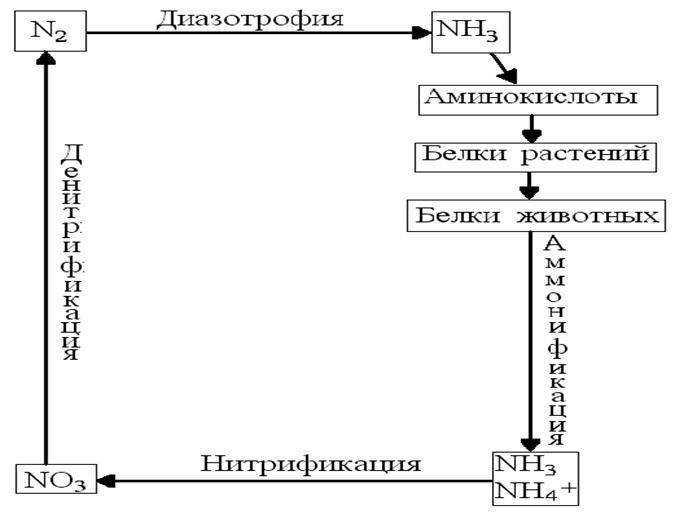 |
Рис. 29 . Круговорот азота в природе
Белки растений и животных могут разлагаться с помощью бактерий─аммонификаторов с образованием аммиака и ионов аммония, затем в процессе микробной нитрификации образуются нитраты. В результате денитрификации образуется молекулярный азот. Все эти превращения происходят с участием микроорганизмов.
Азотофиксация
К азотофиксаторам относят две основные группы бактерий: свободноживущие (ассоциативные) и симбиотические (или клубеньковые) (табл.4).
Таблица 4. Основные группы диазотрофов
|
Свободноживущие (ассоциативные) азотофиксаторы |
Симбиотические азотофиксаторы |
|
ПРЕДСТАВИТЕЛИ |
|
|
Azotobacter, Azospirillium, Klebsiella, Enterobacter, Nostoc, Anabaena, Clostridium |
Симбионты бобовых – Род Rhizobium Симбионты небобовых растений – род Frankia |
|
Обитают в ризосфере, ризоплане растений, обладают Нитрогеназной Активностью, могут в значительной мере заменить минеральный азот, предохраняют от избытка нитратов в продукции. Обладают высокой антибиотической активностью (комплексное питательное и защитное действие) |
Образуют симбиотические клубеньки На корнях растений |
Круговорот азота
Главный источник азота органических соединений – газообразный азот N2 в составе атмосферы. Молекулярный азот не усваивается живыми организмами. Переход его в доступные живым организмам соединения (фиксация) может происходить несколькими путями. Фиксация азота частично происходит в атмосфере, где при грозовых разрядах образуется оксид азота (II), который окисляется до оксида азота (IV), с последующим образованием азотной кислоты и нитратов, выпадающих на поверхность Земли с атмосферными осадками.
Наиболее важной формой фиксации азота является ферментативная фиксация в процессе жизнедеятельности сравнительно немногих видов организмов-азотфиксаторов. Отмирая, они обогащают среду органическим азотом, который быстро минерализуется. Наиболее эффективна фиксация азота, осуществляемая бактериями, формирующими симбиотические связи с бобовыми растениями
Наиболее эффективна фиксация азота, осуществляемая бактериями, формирующими симбиотические связи с бобовыми растениями.
В результате их деятельности в наземных и подземных органах растений (например, клевера или люцерны) за год накапливается азота до 150-400 кг на 1 га. Азот связывают также свободноживущие азотфиксирующие почвенные бактерии, а в водной среде – сине-зеленые водоросли (цианобактерии). Все азотфиксаторы включают азот в состав аммиака (NH3), и он сразу же используется для образования органических веществ, в основном для синтеза белков. Минерализация азотсодержащих органических веществ редуцентами происходит в результате процессов аммонификации и нитрификации.
Аммонифицирующие бактерии в процессе биохимического разложения мертвого органического вещества переводят азот органических соединений в аммиак, который в водном растворе образует ионы аммония (NH4+). В результате деятельности нитрифицирующих бактерий в аэробной среде аммиак окисляется в нитриты (NO2-), а затем в нитраты (NO3-).
Большинство растений получают азот из почвы в виде нитратов. Поступающие в растительную клетку нитраты восстанавливаются до нитритов, а затем до аммиака, после чего азот включается в состав аминокислот, составляющих белки. Часть азота растениями усваивается непосредственно в виде ионов аммония из почвенного раствора.
Животные получают азот по пищевым цепям прямо или опосредованно от растений. Экскреты и мертвые организмы, составляющие основу детритных пищевых цепей, разлагаются и минерализуются организмами-редуцентами, превращающими органический азот в неорганический.
Возвращение азота в атмосферу происходит в результате деятельности бактерий-денитрофикаторов, осуществляющих в анаэробной среде процесс, обратный нитрификации, восстанавливая нитраты до свободного азота.
Значительная часть азота, попадая в океан (в основном со стоком вод с континентов), используется водными фотосинтезирующими организмами, прежде всего фитопланктоном, а затем, попадая в цепи питания животных, частично возвращаются на сушу с продуктами морского промысла или птицами. Небольшая часть азота попадает в морские осадки. Схема круговорота азота приведена на рис.6.
Обогащение почвы
Естественное азотное обогащение почвы – работа исключительно микроорганизмов, в том числе и клубеньковых. До недавнего времени считалось, что только клубеньковые бактерии относятся к микроорганизмам, которые способны фиксировать атмосферный азот из воздуха. Причем ключевую роль в этом процессе играют бобовые растения, поскольку они единственные могут являться симбионтами клубеньковых микробов.
Однако сегодня такая позиция считается устаревшей, поскольку за последнее время найдено огромное количество самых разных бактерий, которые способны превращать молекулярный азот в соединения аммония, а именно аммоний (NH4) уже может усваиваться растениями. Так, например, актиномицеты живут в азотфиксирующем симбиозе как минимум со ста видами деревьев.
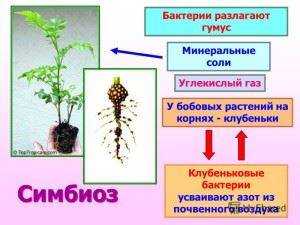
Так как же происходит это обогащение почв:
- Растения, заинтересованные в симбиозе с клубеньковыми бактериями, насыщают почву вокруг своих корней особыми органическими соединениями – флавинами. При этом каждый вид растений вырабатывает индивидуальные и уникальные флавины, на которые реагирует только один вид бактерий. В микробиологии даже названия таким бактериям дают по названию растения, которое для них является напарником по симбиозу.
- Привлеченные флавинами бактерии, способные фиксировать азотные молекулы воздуха, подбираются ближе к корневым волоскам такого растения и, проникая через клеточные стенки покровной ткани корневого волоска, пробираются внутрь корня.
- Проникнув внутрь, бактерии размножаются, а чтобы создать для них достаточное пространство для выполнения возложенной роли, клетки корня начинают делиться и формируют клубенек.
- В процессе своей жизнедеятельности в клубеньке бактерии снабжают растение добытым из воздуха и почв аммонием, а от растения получают углеводы, которые являются для бактерий источником энергии (АТФ).
- Когда растение-симбионт отмирает или сбрасывает листву, его насыщенные аммонием органические ткани попадают в верхние слои почвы и, перегнивая, насыщают это почву азотистыми соединениями в органических молекулах.
- Главная роль этого перегнившего естественного азотного удобрения – стать источником органических азотистых соединений для тех растений, которые впоследствии будут расти на этих почвах, но сами не в состоянии вступить в симбиоз с фиксирующими из воздуха азот бактериями и получить необходимый аммоний напрямую из атмосферы.